Introduzione al gruppo carbonilico
In chimica organica, il gruppo carbonilico è un gruppo funzionale in cui l’atomo di carbonio e ossigeno sono collegati con un doppio legame. I composti contengono gruppo carbonilico sono noti come composti carbonilici. Gruppo carbonile si riferisce ad un monossido di carbonio può anche attaccato ad un atomo inorganico come un ligando che si chiama metallo carbonile, ad esempio nichel carbonile.,
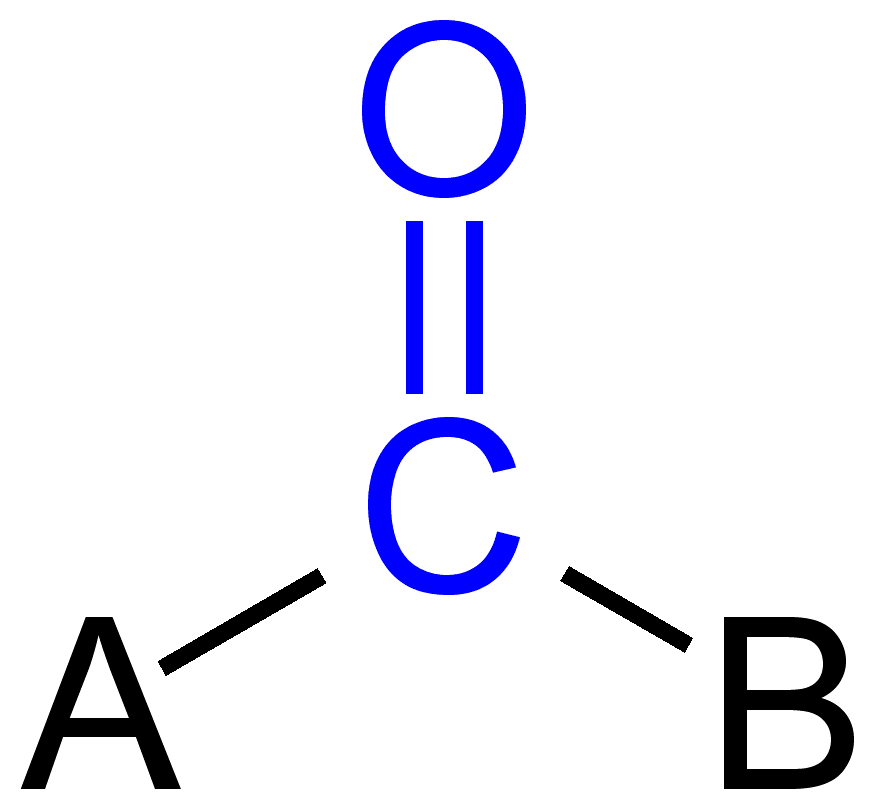
Alcuni gruppi carbonilici
Doppio legame nel gruppo carbonilico
Il carbonio e l’atomo di ossigeno nel gruppo carbonilico sono normalmente ibridati sp2 e quindi plannar. A causa della presenza di ossigeno come atomo elettronegativo, il doppio legame nel gruppo carbonilico è diverso dal doppio legame negli alcheni in termini di reattività. A causa della maggiore elettronegatività e della presenza di due coppie di elettroni solitari, l’ossigeno diventa carica parzialmente negativa mentre il carbonio carbonilico genera carica parzialmente positiva e quindi si osserva la polarità.,
Struttura di risonanza carbonile
A causa della presenza di ossigeno come atomo elettronegativo, il gruppo carbonilico mostra la struttura di risonanza. La struttura di risonanza del gruppo carbonilico influenza la reattività del composto. L’atomo di ossigeno più elettronegativo allontana l’elettrone dal centro del carbonio rende il carbonio carbonilico parzialmente elettropositivo e l’ossigeno parzialmente elettronegativo. Quindi la polarità genera all’interno del composto carbonilico.
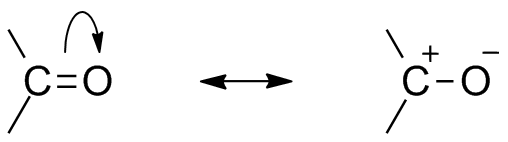
Questo carbonio elettropositivo carbonilico o elettrofilo può ora essere attaccato da un nucleofilo.,
Reattività
Carbonile Alchilazione
Alchilazione del gruppo carbonilico da addizione nucleofila reazione con reagenti di Grignard sono indicati come segue:

proprietà Fisiche dei composti carbonilici
- Il punto di ebollizione di aldeidi e chetoni sono superiori al punto di ebollizione di eteri e alcani di simile massa molecolare.
- Ancora una volta il punto di ebollizione di aldeidi e chetoni sono inferiori ai corrispondenti alcoli.,
- Molte aldeidi superiori hanno un odore gradevole e utilizzate nei profumi o come aromi artificiali mentre il membro inferiore della loro serie omologa ha un odore pungente.
- I chetoni più alti hanno un odore blando e più bassi hanno un odore piacevole, come l’acetone.
- Le piccole aldeidi e chetoni sono solubili in acqua, ma con l’aumentare della lunghezza della catena la solubilità diminuisce.
- Le forze di dispersione di van der Waals diventano più forti man mano che le molecole si allungano.,
H-bonding in carbonil goup
A causa della formazione di H-bonding tra l’ossigeno carbonilico e l’idrogeno della molecola d’acqua, i composti carbonilici inferiori sono solubili in acqua. Ma come la catena aumenta, si arriva sulla strada per formare legame idrogeno e la solubilità diminuisce.
Van der Waals dipolo-dipolo attrazione
A causa della polarità nel gruppo carbonilico e della presenza di forze di dispersione ci sarà un’attrazione tra due molecole vicine. Ciò fa sì che il punto di ebollizione dei composti carbonilici vada più in alto degli alcani corrispondenti., Nella tabella seguente si noti che il punto di ebollizione dei composti carbonilici è superiore agli alcani corrispondenti e inferiore agli alcoli.,v>Boiling point (o C)
Spectroscopy
Infrared spectroscopy
The absorption of carbonyl group depends on the geometry of the molecule., Di solito l’assorbimento di infra luce mostra a at wavenumbers circa 1600-1900 cm-1 (5263 nm a 6250 nm).
Risonanza magnetica nucleare
Il carbonio-NMR del carbonio carbonilico mostra un picco approssimativamente tra 160-220 ppm.
