Tipi di Isomeri Costituzionali Isomeri, Stereoisomeri, Enantiomeri, E Diastereomeri
Come facciamo a dire se le molecole sono “related”? E una volta che sappiamo che sono, come facciamo a capire che tipo di isomero sono?, Sono isomeri costituzionali (stessa formula, connettività diversa), stereoisomeri (stessa connettività, disposizione diversa), enantiomeri (stereoisomeri che sono immagini speculari non sovrapponibili) o diastereomeri (stereoisomeri che NON sono immagini speculari non sovrapponibili.
O sono uguali? :- ) Rispondere a tutte queste domande… e molto altro ancora!
Sommario
- “Come siamo relazionati, di nuovo?”- Come gli isomeri sono come i membri della famiglia
- I tipi di relazioni tra molecole
- Come distinguere una coppia di non-isomeri vs., Una Coppia Di Isomeri
- Tipi Di Isomeri Costituzionali Isomeri Sono Diversi Connectivites
- Tipi Di Isomeri: Stereoisomeri Hanno La Stessa Connettività, Ma con Una Diversa Disposizione Dei Loro Atomi Nello Spazio
- Stereogenici “Elementi” In Stereoisomeri
- Tipi Di Stereoisomeri: Enantiomeri vs. Non-Enantiomeri (un.k.un. Diastereomeri)
- Cosa Significa “Non Sovrapponibili Immagine Speculare” Anche Significare??,
- Proprietà Fratelli Stagione 13 Episodio 13: “il Signore Voldemort, E La Proprietà Di Chiralità”
- Enantiomeri Hanno Identiche Proprietà Fisiche Tranne che per Rotazione Ottica
- Il Terzo di Proprietà Fratello”: meso-Acido Tartarico
- Solo Molecole Chirali Può Avere Enantiomeri
- Diastereomeri Sono Stereoisomeri Che Non Sono Enantiomeri
- Diastereomeri Hanno Differenti Proprietà Fisiche
- Un Modo Rapido Per capire Se Due Stereoisomeri Sono Diastereomeri
- Guardare Fuori Per le Domande di Trucco!,
- Sommario: Tipi di isomeri
- Note
” Come ci relazioniamo di nuovo?”- Come gli isomeri sono come i membri della famiglia
Poche settimane fa, in una riunione di famiglia in Ontario, ho presentato i miei parenti alla gioia del gelato all’azoto liquido. I miei cugini erano lì, come molti dei loro figli. Così erano alcuni dei miei cugini papà. Essendo una riunione di famiglia, hanno invitato i loro figli (cresciuti), che a loro volta hanno portato i loro figli. Mentre servivo loro il gelato, nella foschia del vapore dell’azoto liquido mi chiedevo: “sono questi i miei cugini di terzo grado? O i miei cugini di secondo grado una volta rimossi…?,”
Merda, mi dimentico. Come funziona di nuovo questa cosa del cugino?
In chimica organica, possiamo anche trovarci sconcertanti su domande come “come sono correlate queste due (o più) molecole”? E proprio come la terminologia familiare, ricordare le distinzioni tra isomeri costituzionali, stereoisomeri, enantiomeri e simili può essere una lotta all’inizio.
In questo post, cerchiamo di mostrare come rispondere a domande come:
- Queste due molecole sono isomeri? (e quali sono gli isomeri, comunque?,)
- Questi due isomeri sono isomeri costituzionali o stereoisomeri (e qual è la differenza?)
- Questi due stereoisomeri sono enantiomeri o diastereomeri (e cosa significa?)
Per fortuna la risposta a ciascuna di queste domande è molto chiara, e spero che scoprirai che con la pratica (e alcuni esempi vividi) sono più facili da ricordare rispetto all’intera cosa di terzo cugino contro cugino di secondo grado.,
I tipi di relazioni tra molecole
Una molecola può essere diversi tipi di isomero allo stesso tempo, a seconda di quale molecola si sta confrontando.
Per usare la nostra analogia familiare: i termini “fratello”, “sorella”, “madre”, “figlia” sono parole che descrivono le relazioni tra (almeno) due persone. Puoi essere una figlia (a tua madre), una sorella (a tuo fratello), un cugino (a tua zia & figli degli zii) e “non correlati” (a me) tutti allo stesso tempo.,
Chiedere se sei una figlia O una sorella non ha senso senza il contesto di includere la persona “a CUI” condividi quella relazione.
Così è con le molecole. Una molecola può essere un isomero costituzionale, diastereomero, enantiomero e altro (o nessuno!), tutti allo stesso tempo a diverse molecole, a seconda di quale altra molecola(s) si sta confrontando.
Ci sono tre importanti distinzioni da imparare, e le attraverseremo ciascuna a turno.,
- Una determinata coppia di molecole che possono essere isomeri O non isomeri
- Una determinata coppia di isomeri possono essere isomeri costituzionali O stereoisomeri
- Una determinata coppia di stereoisomeri può essere enantiomeri O diastereomeri
(esami, in particolare, c’è sempre la possibilità che un “data coppia di molecole” è in realtà la stessa molecola, disegnato in modo diverso. Copriremo anche questa possibilità).,
Il diagramma di flusso si presenta così:
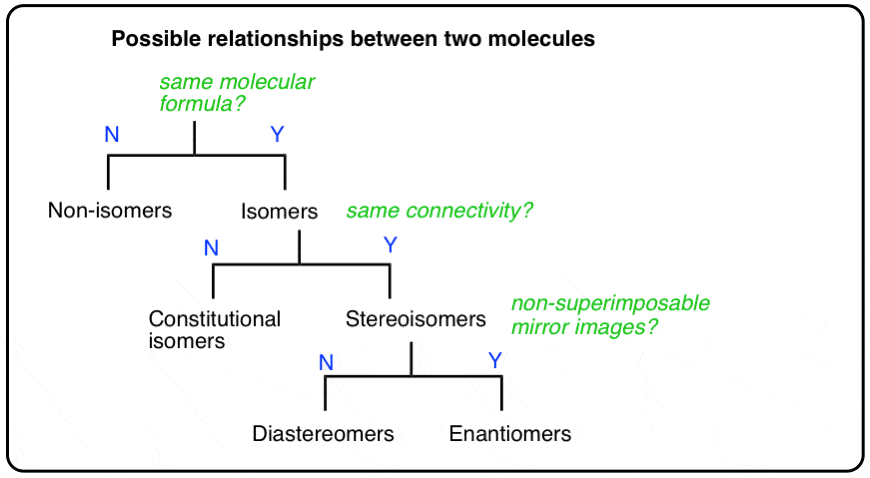
Una differenza fondamentale tra famiglie e molecole:
Attraverso le circostanze lascerò al lettore di capire, è possibile che qualcuno sia contemporaneamente padre e fratello per lo stesso individuo.
Per fortuna, non abbiamo tali problemi in chimica organica.
Due molecole potrebbero essere stereoisomeri l’una dell’altra, ma non possono essere stereoisomeri e isomeri costituzionali l’una dell’altra. Le distinzioni sono chiare.
Come distinguere una coppia di non-isomeri vs., Una coppia di isomeri
Isomeri sono due (o più) molecole che condividono la stessa formula molecolare.
Per alcune formule molecolari, non esistono isomeri. Ad esempio, esiste un solo isomero possibile per CH4 (metano), C2H6 (etano) e propano (C3H8), e solo due sono possibili per C4H10 (2-metilpropano e n-butano).
All’aumentare del numero di atomi di carbonio, tuttavia, aumenta anche il numero di possibili isomeri. Per dodecano (C12H26), sono possibili 355 isomeri. E va solo da lì!,
Nonostante condividano le stesse formule molecolari, gli isomeri possono avere proprietà fisiche molto diverse, come il punto di ebollizione, il punto di fusione e la reattività chimica.
Prendere cicloesano (b.p. 63 °C) e 1-esene (80 °C) che hanno entrambi la formula molecolare C6H12. Non importa quanto siano diverse le loro proprietà fisiche, o le loro reattività, la loro formula molecolare comune li rende isomeri l’uno dell’altro.,
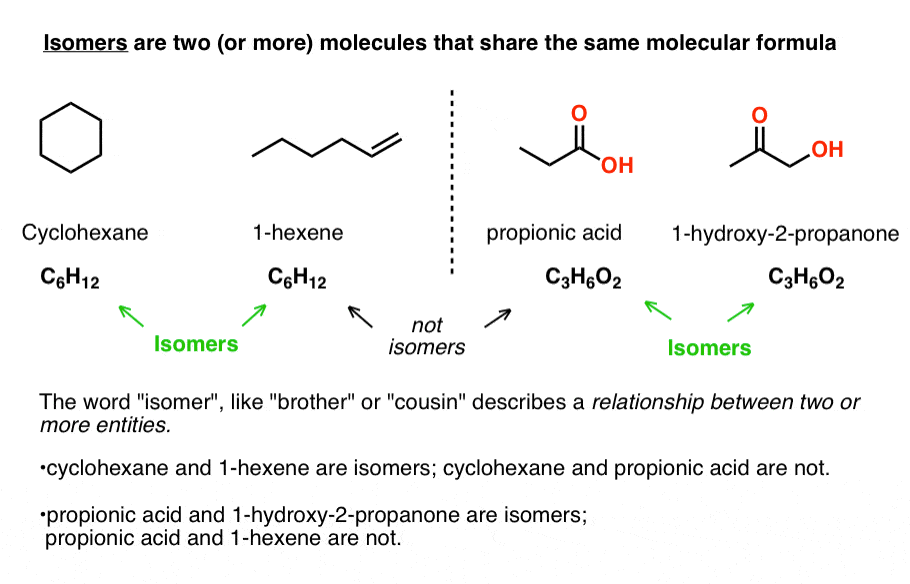
Allo stesso modo, l’acido propionico e l ‘ 1-idrossi-2-propanone condividono la stessa formula molecolare, C3H6O2, rendendoli isomeri l’uno dell’altro (ma non isomeri di cicloesano o 1-esene, ovviamente!).

Questo ci porta alla domanda successiva. Diciamo che due molecole date sono isomeri. Che tipo di isomero sono?
Gli isomeri si dividono ordinatamente in due categorie: isomeri costituzionali (connettività diversa) e stereoisomeri (stessa connettività, diversa disposizione nello spazio). Quindi cosa significa in realtà?
4., Tipi di isomeri: Gli isomeri costituzionali hanno diversi Connectiviti
Gli isomeri costituzionali hanno la stessa formula molecolare, ma diverse connettività.
Le stesse parti, ma disposte in modi diversi. Per prendere questo esempio vecchio ma buono, cambia una coda e una gamba e fai isocats:

È divertente, ma c’è un modo più rigoroso di pensare alla connettività?
Mi capita di trovare utile la seguente regola empirica:
Gli isomeri costituzionali hanno le stesse formule empiriche ma i loro nomi IUPAC principali sono diversi.,
A titolo di esempio, queste 5 molecole sono tutti isomeri costituzionali l’uno dell’altro. Hanno la stessa formula empirica (C6H12) ma connettività diversa. Nota come anche i nomi IUPAC sono completamente diversi.
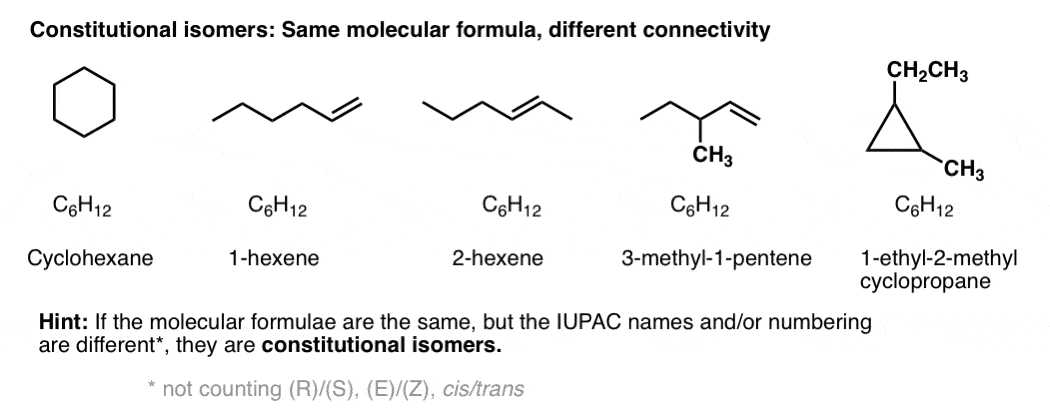
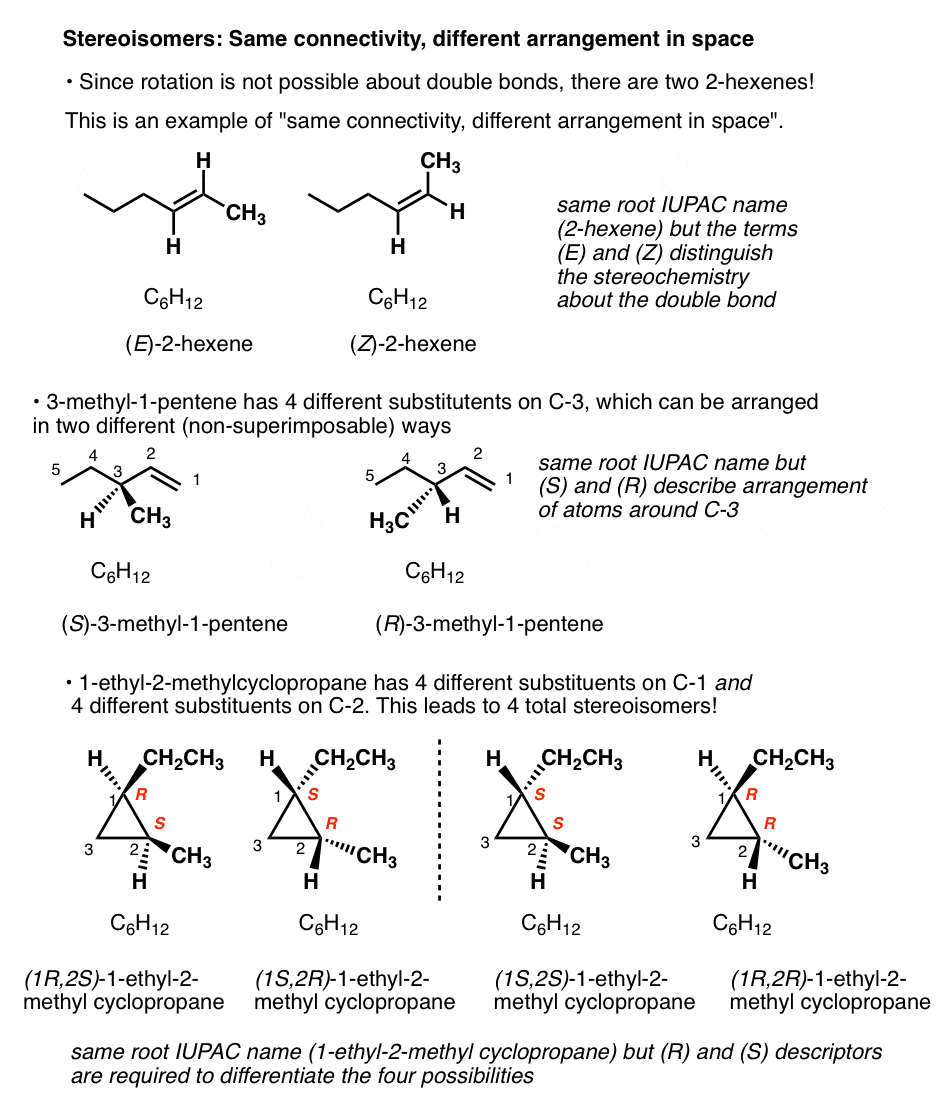
Tipi Di Isomeri: Stereoisomeri Hanno La Stessa Connettività, Ma con Una Diversa Disposizione Dei Loro Atomi Nello Spazio
C’è un solo modo per collegare C6H12 insieme per formare il cicloesano, e solo un modo per collegare gli stessi atomi insieme per ottenere 1-hexene.,
Ma ci sono due modi per collegare C6H12PER dare molecole con i nomi 2-esene e 3-metil-1-pentene! E quattro modi per collegare C6H12 per dare 1-etil-2-metilciclopropano!
(Modo rapido per identificare un chimico organico ben addestrato: chiedere loro di disegnare 2-esene e misurare quanto velocemente ci vuole per dire “quale”?).
Ad esempio: ci sono due modi per disporre gli idrogeni sul doppio legame del 2-esene; quando sono sullo stesso lato, ci riferiamo ad esso come cis (o Z); sul lato opposto, trans (E). .,
Poiché la rotazione libera attorno al doppio legame non è possibile, queste sono molecole completamente distinte. Possono essere separati, messi in diversi flaconi, lasciati sullo scaffale per anni e mai interconvertiti. È possibile acquistare cis-2-esene (95%) da Aldrich, lasciarlo nel magazzino per due decenni e non temere mai che si sia trasformato nella forma trans.
Che tipo di isomeri sono questi? Non possiamo chiamarli isomeri costituzionali, dal momento che hanno la stessa connettività (entrambi sono 2-esene! ). Ci serve un altro nome., Poiché differiscono nella disposizione dei loro gruppi nello spazio sul doppio legame li chiamiamo stereoisomeri.
Gli stereoisomeri possono anche derivare da atomi di carbonio tetraedrici che sono attaccati a quattro diversi sostituenti (cioè un carbonio “chirale” o “asimmetrico”) come nel 3-metil-1-pentene. Ci sono 2 (e solo 2!) diversi modi di organizzare quattro diversi gruppi attorno a un centro tetraedrico, che dà origine a due molecole che condividono la stessa connettività ma differiscono nella disposizione dei loro atomi nello spazio., Queste molecole possono avere lo stesso aspetto, ma sono in realtà immagini speculari non sovrapponibili (più su che alcuni paragrafi sotto).
Stereogenici “Elementi” In Stereoisomeri
Un doppio legame in grado di cis/trans isomeria come pure di una “asimmetrico” atomo di carbonio sono a volte chiamati “elementi stereogenici”, dal momento che ognuno di loro danno origine ad un paio di stereoisomeri (E, Z), o (R o S)
- Una molecola che ha 2 elementi stereogenici possono dare origine a (2 × 2) = 4 diversi stereoisomeri. Questo è il caso di 1-etil-2-metil ciclopropano: (R, R), (S, S), (R, S) e (S,R).,
- Una molecola con 3 elementi stereogenici può dare origine a ben (2 × 2 × 2) = 8 diversi stereoisomeri.
- Generalmente, una molecola con n elementi stereogenici può avere fino a 2n stereoisomeri. (Probabilmente l’esempio più pazzo conosciuto in chimica è la palitossina, che ha 64 centri chirali, 8 doppi legami e circa 1021 possibili stereoisomeri. )
Un modo rapido per capire se due molecole sono stereoisomeri è se hanno lo stesso nome core IUPAC ma differiscono nelle loro designazioni cis/trans, E/Z o (R)/(S).
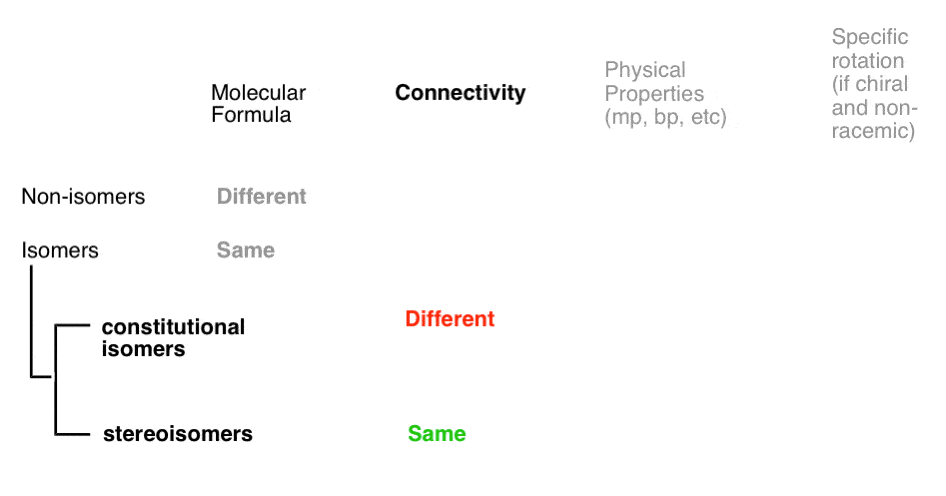
7., Tipi di Stereoisomeri: Enantiomeri vs. Non-Enantiomeri (alias Diastereomeri)
Non abbiamo ancora finito. C’è un’ultima importante distinzione da fare tra due diversi tipi di stereoisomeri.
Perché?, Beh, per spingere la nostra famiglia analogia solo un po ‘ di più… parliamo di fratelli:

(sì, c’è un terzo Fratello)
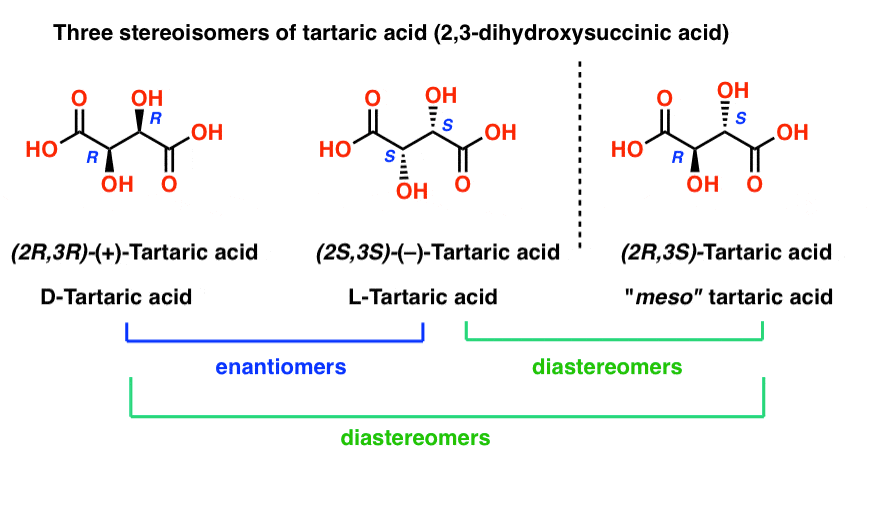
Questi tre uomini sono tutti fratelli, ma chiaramente c’è qualcosa di speciale il rapporto tra due dei tre che merita di categoria:
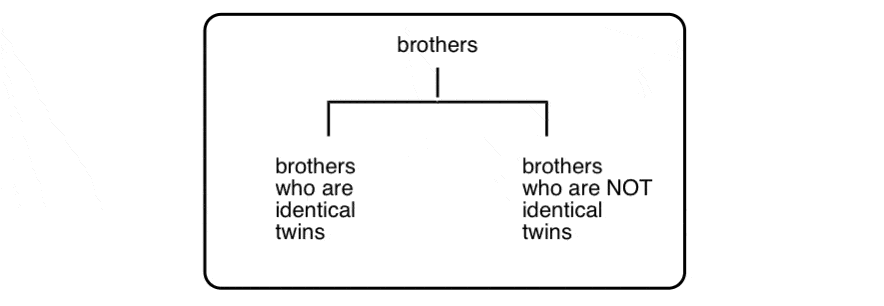
Questo non è come la distinzione tra diastereomeri (stereoisomeri che NON SONO non sovrapponibili immagini speculari) e enantiomeri (stereoisomeri che non SONO sovrapponibili immagini speculari).,
Cosa significa anche “Immagine speculare non sovrapponibile”??
Ammetto: il termine “immagini speculari non sovrapponibili” sembra dare alle persone tanti problemi quanto la cosa “cugino di secondo grado rispetto a una volta rimossa”. Quindi affrontiamo questo adesso.
Nella nostra analogia familiare (sopra) abbiamo fatto “fratelli che sono gemelli identici” analoghi agli enantiomeri e “fratelli che non sono gemelli identici” analoghi ai diastereomeri.
Dobbiamo modificare un po ‘ questa analogia.
In chimica organica, due molecole che possono essere sovrapposte l’una sull’altra, attraverso la rotazione dei legami (cioè, i cambiamenti conformazionali) o attraverso la rotazione della molecola stessa, sono considerati la stessa molecola.
In altre parole, in chimica organica, le molecole che sono “gemelli identici” non sono isomeri; sono considerate copie identiche della stessa molecola.
Una talpa, dopo tutto, è 6,02 × 1023 molecole identiche e sovrapponibili., E proprio come i gemelli identici sono ancora identiche se uno è seduto ad una scrivania di ricerca immobiliare che nella vostra fascia di prezzo, mentre l’altro è in piedi in un pessimo cucina gesticolando con le mani, cercando di mostrare come si può essere completamente ristrutturato per misura il vostro budget, le molecole sono ancora considerati “identici” se capita di essere in diverse conformazioni, così a lungo come ognuno di passare attraverso almeno una conformazione in cui sono sovrapponibili.,
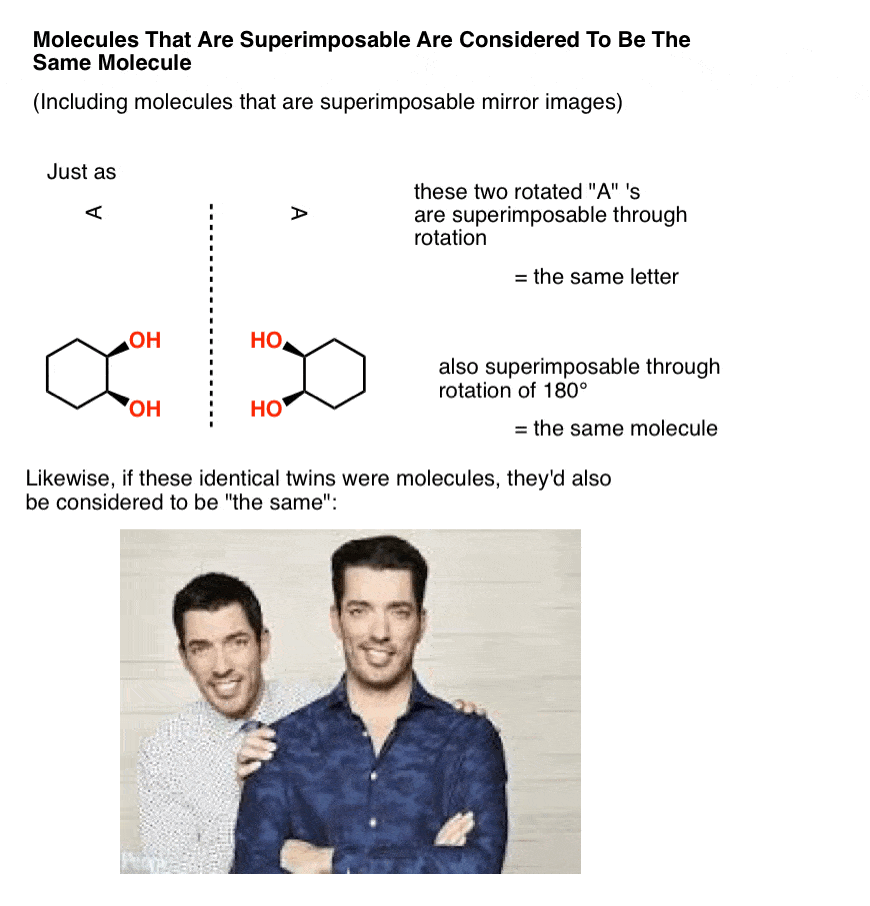
Ora, facciamo una piccola modifica ai nostri gemelli identici in modo che passino dall’essere immagini speculari sovrapponibili (= uguali) a immagini speculari non sovrapponibili.
Property Brothers Stagione 13, Episodio 13: “Lord Voldemort e la proprietà di Chirality”
NARRATORE: Il nostro cliente, “Lord Voldemort” ha detto che stava cercando una nuova tana malvagia con “buone ossa”, quindi lo abbiamo portato in città per guardare alcune proprietà che si adattano alla sua lista di “must have” e budget. Più tardi quella sera, dopo un paio di drink, le cose sono diventate imbarazzanti.,
LORD VOLDEMORT: Ehi ragazzi, in realtà ho una nuova proprietà che potrebbe interessarvi
DREW E JON: Gesù! Che diavolo è quel sottile –
LV: La proprietà della CHIRALITÀ! Racemundum suorum!
ZAP! (flash di luce)
DREW E JON: Aaarrrggh!!
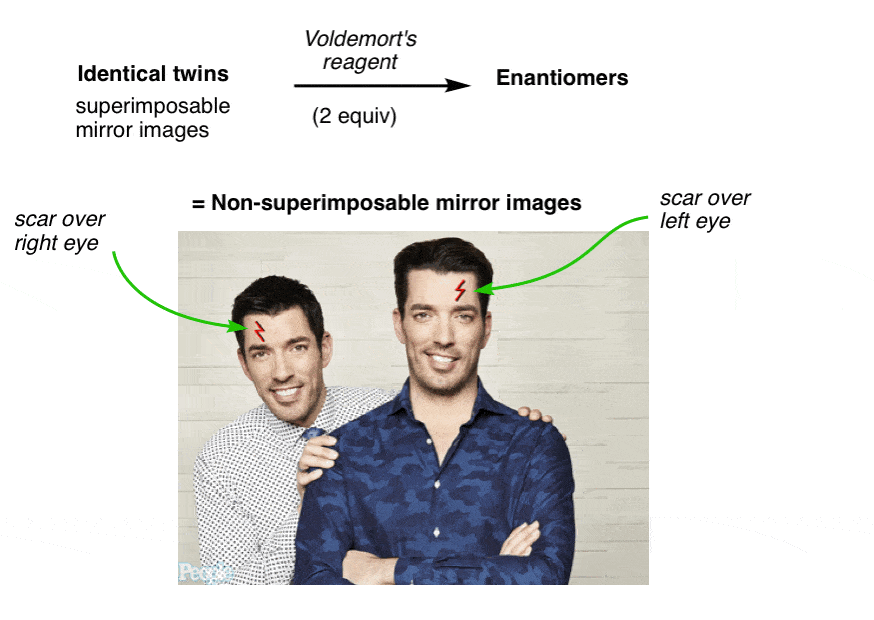
Uno ha una cicatrice sull’occhio sinistro e l’altro ha una cicatrice sulla destra. Nessuna quantità di torsione e tornitura sul pavimento nel dolore può forse renderli sovrapponibili ora.
Sono diventati “enantiomeri”: immagini speculari non sovrapponibili.,
Poiché non sono più sovrapponibili, in termini chimici non sono più gli stessi. Simile, sì! Ma non la stessa molecola.
Cosa è cambiato?
Reagente di Voldemort
Prima di aggiungere il reagente di Voldemort, ogni gemello aveva un piano di simmetria lungo il centro del suo corpo tale che le metà sinistra e destra erano identiche. Basta. Ora la metà sinistra di ogni gemello è diversa dalla metà destra. Chiamiamo questa proprietà “asimmetria”o “chiralità”.
L’introduzione della cicatrice “ha rotto la simmetria” di ogni gemello e ha introdotto la chiralità.,

Con le molecole, il modo più comune per impartire chiralità è con un cuscinetto di carbonio 4 diversi gruppi, come in 4-metil-1-pentene, sopra. Per questo motivo un carbonio collegato a 4 gruppi diversi è chiamato un centro chirale, o”centro asimmetrico”.
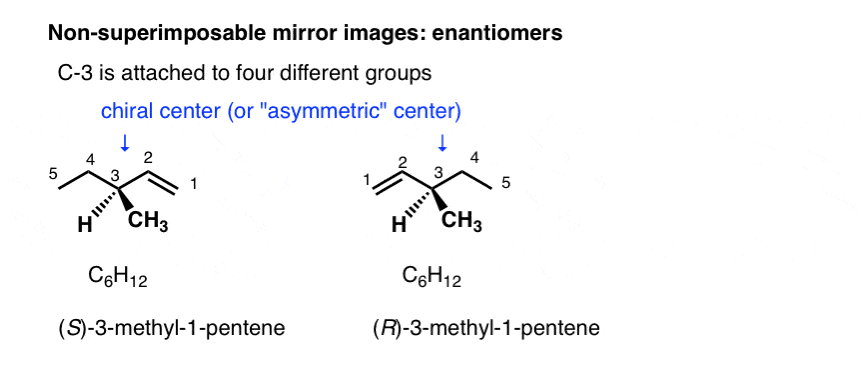
Ce ne sono due (e solo due!) modi per disporre 4 diversi sostituenti attorno a un carbonio tetraedrico. Quindi una molecola con un singolo centro asimmetrico esisterà come una coppia di stereoisomeri., Per essere più specifici, esisterà come una coppia di immagini speculari non sovrapponibili: enantiomeri.
Gli enantiomeri hanno proprietà fisiche identiche Tranne che per la rotazione ottica
In precedenza abbiamo descritto le avventure di Louis Pasteur con l’acido tartarico dove ha scoperto che un composto allora noto come “acido racemico” (dal latino racemus = “un grappolo d’uva”) era in realtà una miscela uguale di due forme speculari di acido tartarico.
Separare questi due isomeri era un inferno su ruote, poiché hanno solubilità identiche, punti di fusione e altre proprietà fisiche., Pasteur è stato in grado di realizzarlo solo attraverso l’osservazione di piccole differenze nelle apparenze dei loro sali, e li raccolse a parte con una pinzetta e una lente d’ingrandimento.
L’unica proprietà fisica che differenzia questi due isomeri è che ruotano il piano della luce polarizzata in direzioni uguali e opposte.
Con il senno di poi, ora conosciamo le strutture di questi due isomeri dell’acido tartarico, e usando le regole di Cahn-Ingold-Prelog, li abbiamo chiamati (R,R) e (S,S) acido tartarico.
Questi due isomeri sono immagini speculari l’una dell’altra: immagini speculari non sovrapponibili.,
Proprio come con il posizionamento delle cicatrici di Voldemort, nessuna quantità di rotazione del legame può trasformare una configurazione (R) in una configurazione (S), o viceversa.
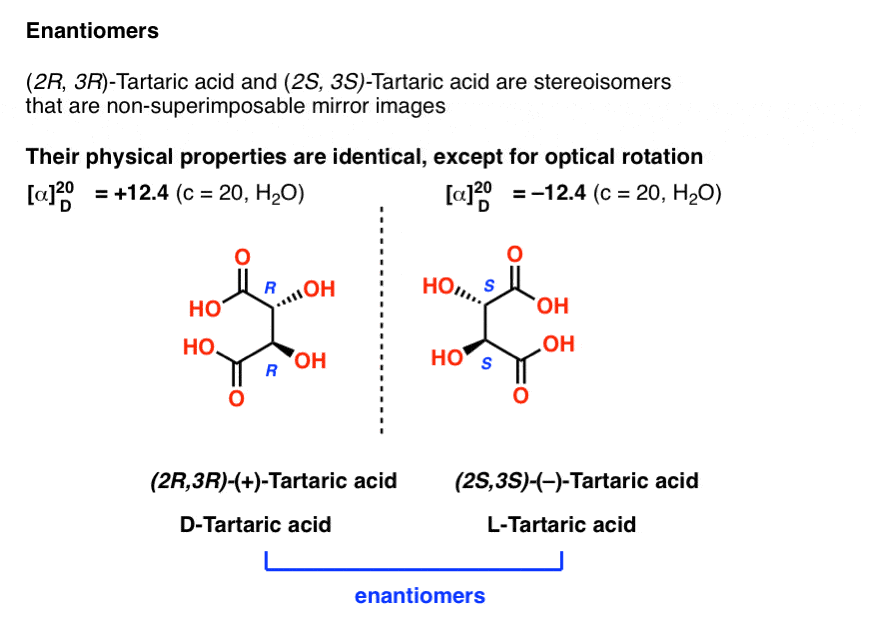
Questo è un indizio importante per identificare gli enantiomeri (e ne parleremo ulteriormente in un post futuro):
Gli enantiomeri avranno sempre gli stessi nomi IUPAC e descrittori completamente opposti (R / S).,
“Il terzo fratello di proprietà”: acido meso-tartarico
L’acido tartarico ha due centri di carbonio asimmetrici, e abbiamo detto prima che una molecola con due centri asimmetrici può avere fino a 22 = 4 stereoisomeri. Se (2S, 3S) e (2R,3R) sono due stereoisomeri dell’acido tartarico, allora che dire dell’acido tartarico (2R, 3S) e (2S, 3R)? Questi dovrebbero anche essere stereoisomeri, giusto?
Quando disegniamo le strutture di (2R,3S) e (2S,3R) acido tartarico, tuttavia, qualcosa diventa rapidamente evidente.,
Mentre sono effettivamente immagini speculari l’una dell’altra, sono immagini speculari l’una dell’altra nello stesso modo in cui i nostri gemelli identici (pre-Voldemort) sono immagini speculari l’una dell’altra:
Sono immagini speculari sovrapponibili, e quindi considerate molecole identiche.
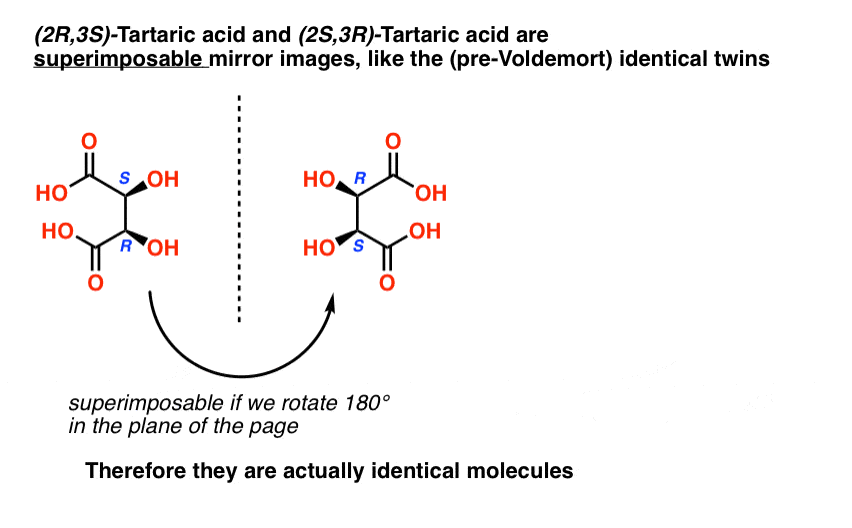
Pertanto (2R, 3S)-acido tartarico e (2S, 3R)-acido tartarico non sono enantiomeri. Sono in realtà due modi diversi di descrivere la stessa molecola, e l’acido tartarico ha solo tre stereoisomeri complessivi.
Aspetta., Come può essere che una molecola possa avere centri chirali ma non avere un enantiomero?
12. Solo le molecole chirali possono avere Enantiomeri
Proprio nello stesso modo in cui il nostro fratello di proprietà (pre-Voldemort) aveva orecchie (chirali) sinistra e destra, ma era achirale nel complesso a causa del piano specchio interno. Solo le molecole chirali possono avere enantiomeri.
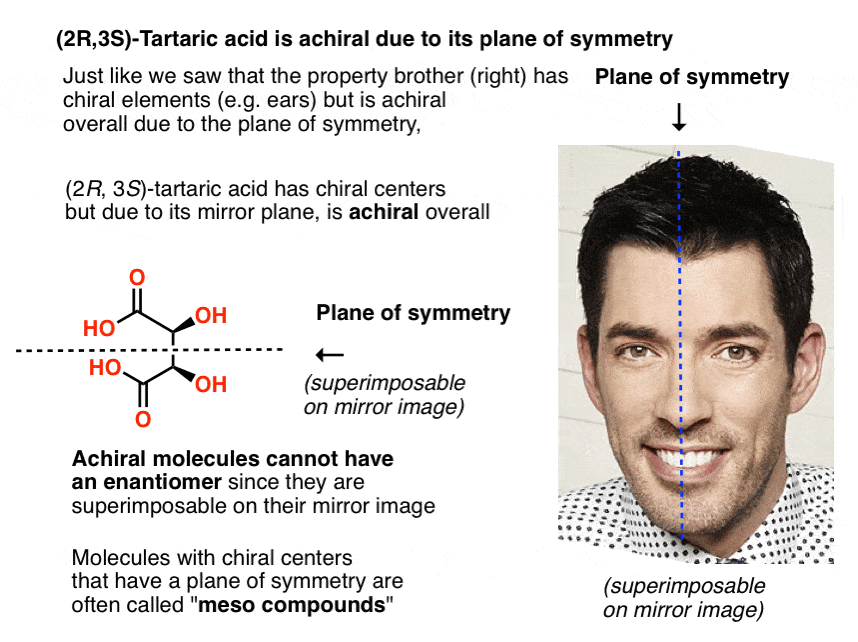
Una molecola con un piano specchio interno – un piano di simmetria – è achirale e non avrà un enantiomero.
Allo stesso modo, (2R, 3S)-l’acido tartarico ha centri chirali, ma possiede un piano specchio interno., Il centro chirale con la configurazione S è l’immagine speculare del centro chirale con la configurazione R, e gli altri sostituenti sono disposti simmetricamente.
Questo stereoisomero dell’acido tartarico era noto a Pasteur, poiché poteva essere facilmente separato dall’acido tartarico “racemico” a causa delle sue diverse proprietà fisiche (solubilità). Poiché la sua rotazione specifica (0°) era in” mezzo “(meso = ” medio ” in greco) tra levo (–) e dextro (+) acido tartarico, è stato dato il nome di acido meso-tartarico.,
Sapendo cosa facciamo ora, ha senso che l’acido meso-tartarico ha una rotazione specifica di 0°, poiché solo le molecole chirali ruotano il piano della luce polarizzata, e l’acido meso-tartarico è achirale.
Il nome “meso” è stato adottato più in generale. Un “composto meso” è una molecola che ha centri chirali, ma è nel complesso achirale a causa della presenza di un piano specchio interno.
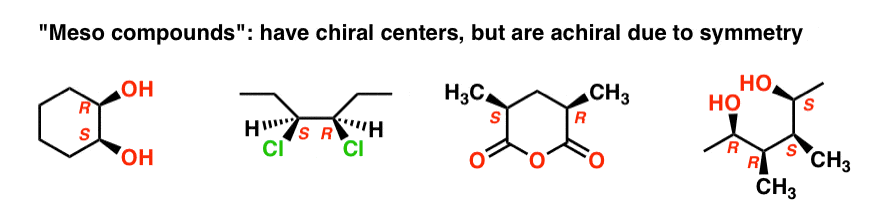
Questo è il motivo per cui è stato utilizzato il qualificatore “fino a 22 stereoisomeri”., Una molecola con 2 stereocentri può avere ” fino a ” 4 stereoisomeri, ma può avere meno di 4 se è presente una forma meso.
l’acido meso-tartarico è un po ‘ come il terzo fratello di proprietà: “colui che non è un gemello”.
I diastereomeri sono stereoisomeri che non sono Enantiomeri
Quindi se (2R, 3R)-acido tartarico e (2S, 3S)-acido tartarico sono enantiomeri, come descriviamo la relazione tra ciascuna di queste molecole e l’acido meso-tartarico?
In chimica organica, chiamiamo “stereoisomeri che non sono enantiomeri”, diastereomeri.,
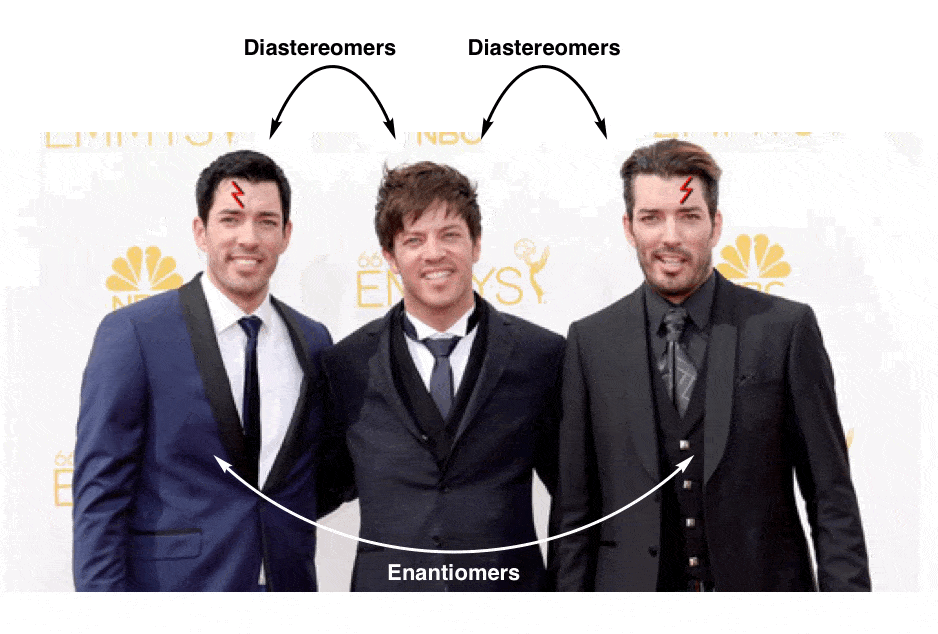
meso-acido tartarico è un diastereoisomero di entrambi (2R,3R)-tartarico, acido (2S, 3S)-acido tartarico:
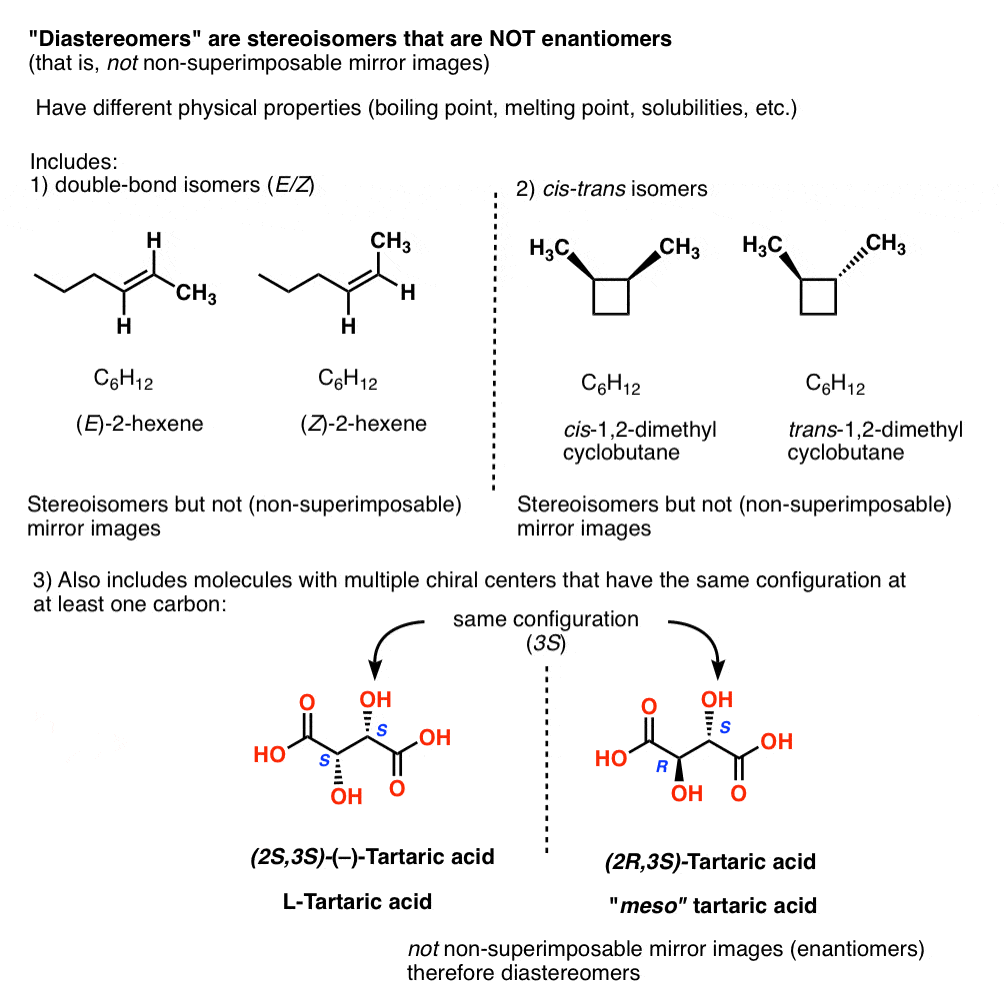
Altri esempi di “diastereomeri” includono:
- doppio legame isomeri (E/Z)
- cis–trans isomeri
- stereoisomeri di molecole con più centri chirali che hanno la stessa configurazione (almeno) uno di carbonio
14., I diastereomeri hanno proprietà fisiche diverse
Proprio come Pasteur ha trovato l’acido meso-tartarico relativamente facile da separare dall’acido “racemico”-tartarico, i diastereomeri hanno proprietà fisiche diverse (ad esempio punto di ebollizione, punto di fusione, solubilità, ecc.).
15. Un modo rapido per dire se due stereoisomeri sono Diastereomeri
Un modo rapido per dire se due stereoisomeri sono diastereomeri:
- se due stereoisomeri differiscono nei descrittori cis/trans o E/Z (ad es., cis-2-esene e trans-2-esene)
- se hanno almeno un descrittore R/S identico (come in (2S,3S)-acido tartarico e (2R, 3S)-acido tartarico (se tutti i descrittori R/S sono uguali, devono differire in qualche modo nell’orientamento cis/trans o E/Z per essere diastereomeri; altrimenti sono la stessa molecola!)
16. Attenzione per le domande trabocchetto!
Ultimo esempio, prometto.
Prendi le due molecole sottostanti. Sono isomeri? Se sì, che tipo di isomero sono?,
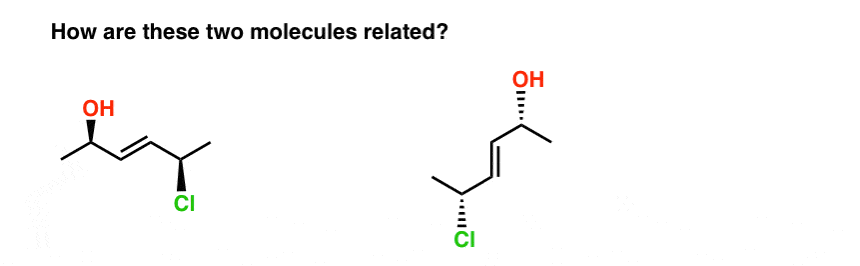
Il modo più veloce che conosco per rispondere a questa domanda è provare a nominarli entrambi.
Quando facciamo questo, troviamo che:
- la molecola a sinistra è E-(2R, 5R)-5-chloro-hex-3-en-2-ol
- la molecola a destra è E – (2R, 5R)-5-chloro-hex-3-en-2-ol
Quindi come sono correlati?
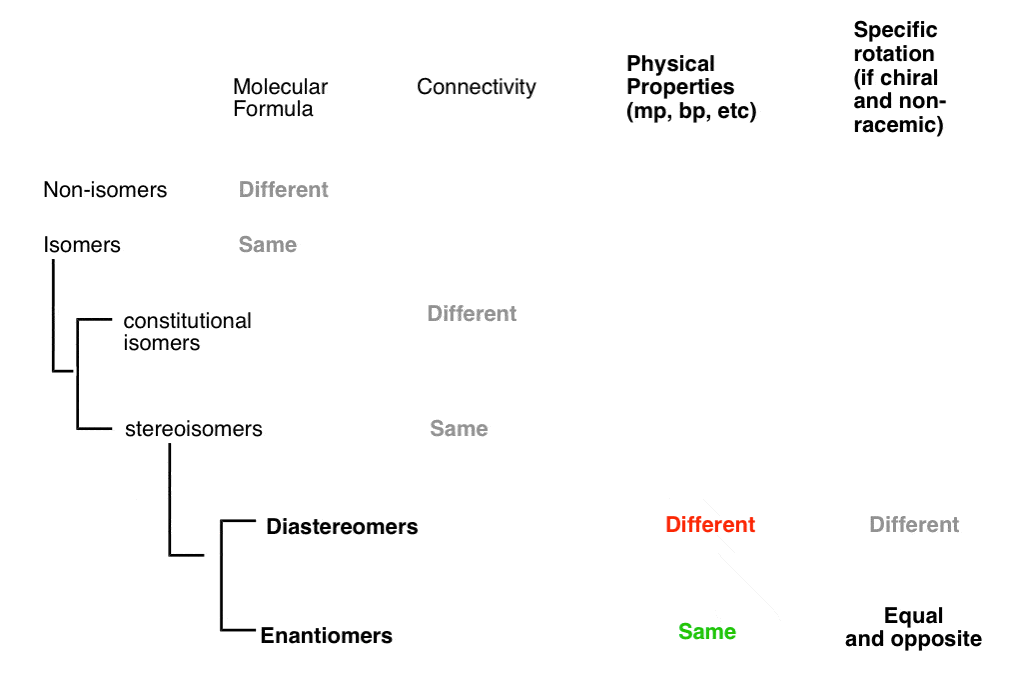
- Non sono isomeri costituzionali (stessa connettività!)
- Ma non sono neanche stereoisomeri (stessi descrittori E/Z e R/S !)
Quindi Therefore sono uguali!, (In realtà, sono diverse conformazioni della stessa molecola, e facciamo l’ipotesi che tutte le conformazioni della stessa molecola siano interconvertibili, a meno che non venga detto diversamente. ) cfr.nota a piè di pagina.
17. Sommario: Tipi di isomeri
Questo è stato un post lungo, ma si spera completo e illuminante sui tipi di isomeri.
Nella prossima puntata impareremo una tecnica che – con la pratica – vi permetterà di determinare rapidamente se le molecole sono enantiomeri, diastereomeri, o gli stessi.
Grazie ancora a Matt per la co-creazione., Chiedi a Matt di programmare una sessione di tutoraggio online qui.
Note
Nota a piè di pagina – atropisomeri
Generalmente si assume che gli isomeri conformazionali interconvertano rapidamente sulla scala temporale necessaria per misurare la rotazione ottica.
Ad esempio, le due forme di sedia di cis-1,2-dimetilcicloesano sono in realtà enantiomeri, ma poiché si interconvertono così rapidamente a temperatura ambiente, vengono trattate come se fossero uguali.,
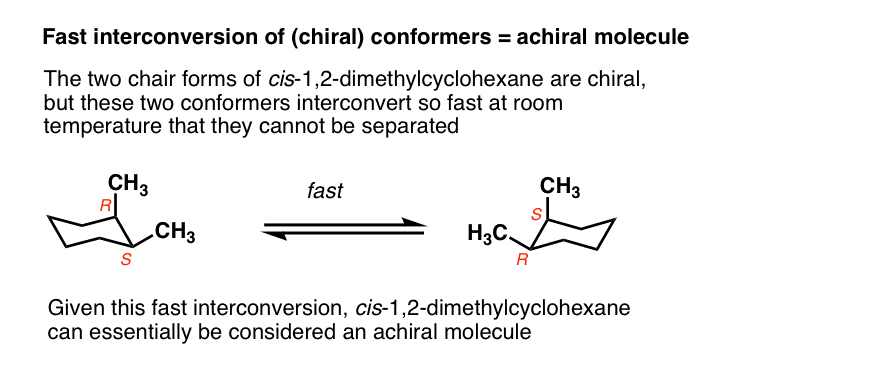
Questo di solito va oltre lo scopo della chimica organica introduttiva, ma ci sono alcuni casi in cui questa ipotesi non è valida.
Un esempio importante è 1,1-bi-2-naftolo (aka BINOL).
Il conformer A (all’estrema sinistra) non può convertirsi in conformer B (all’estrema destra) senza passare attraverso una conformazione in cui i due anelli sono complanari (al centro) e i due idrogeni su ciascun carbonio (carbonio 8) si scontrano l’uno con l’altro., Questo presenta una barriera abbastanza grande alla rotazione che ciascuna di queste due conformazioni è “intrappolata” nel proprio stato a temperatura ambiente e non si interconverte.
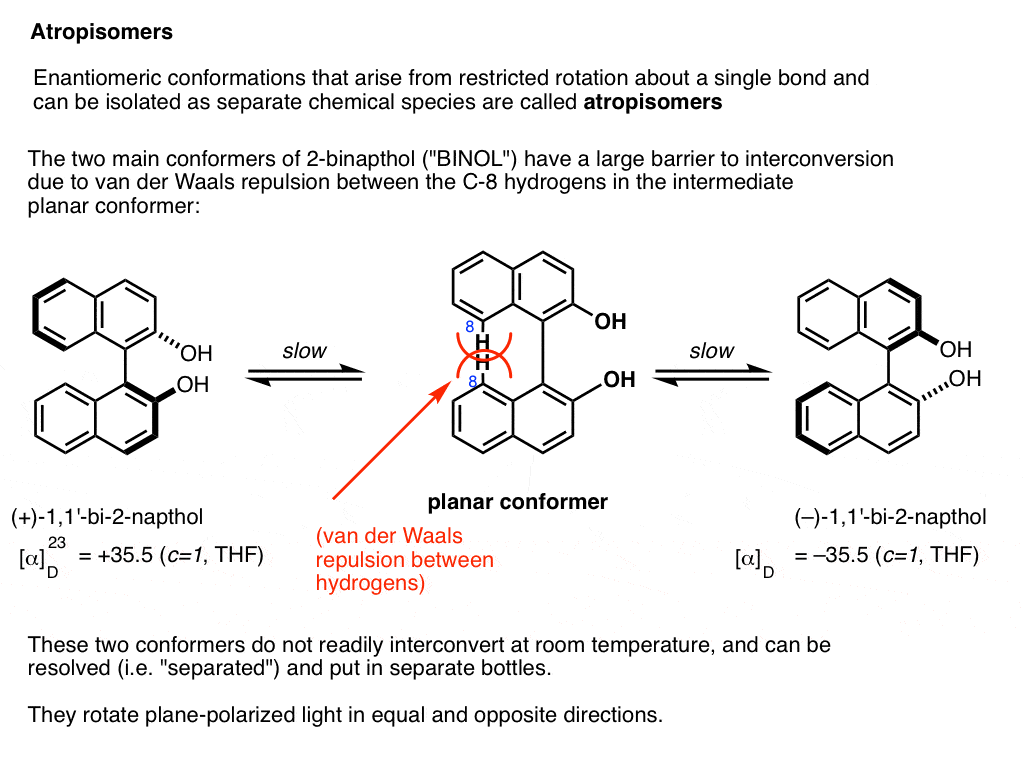
Queste due conformazioni sono immagini speculari non sovrapponibili l’una dell’altra allo stesso modo in cui una vite mancina e una destrorsa sono immagini speculari non sovrapponibili l’una dell’altra. Si dice che abbiano un “asse di chiralità”.
La barriera tra i due conformer è abbastanza grande che il conformer A e il conformer B possono essere risolti (separati) e messi in bottiglie diverse.,
Questo caso speciale di conformatori isolabili è chiamato “atropisomerismo”.
