Alte Serii
\
valorile pentru \(n_2\) și număr de undă \(\widetilde{\nu}\) pentru această serie ar fi:
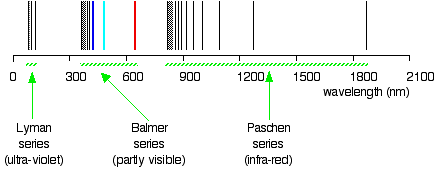
știi în ce regiune de radiatii electromagnetice, aceste linii sunt? Desigur, aceste linii sunt în regiunea UV și nu sunt vizibile, dar sunt detectate de instrumente; aceste linii formează o serie Lyman., Existența seriei Lyman și a seriei lui Balmer sugerează existența mai multor serii. De exemplu, seria cu \(n_2 = 3\) și \(n_1\) = 4, 5, 6, 7, … se numește seria Pashen.
Mulitple seria
Exemplu \(\PageIndex{1}\): Lyman Seria
așa-numita Lyman serie de linii în spectrul de emisie al hidrogenului corespunde tranzițiilor de la diferite stări excitate la n = 1 orbită. Calculați lungimea de undă a liniei cu cea mai mică energie din seria Lyman la trei cifre semnificative. În ce regiune a spectrului electromagnetic apare?,
Având în vedere: mai mic de energie orbită în seria Lyman
Cerut: lungime de undă cu cel mai mic de energie Lyman linie și regiunea corespunzătoare a spectrului
Strategie:
Rezolvare:
putem folosi Rydberg ecuația (Ecuația \ref{1.5.1}) să se calculeze lungimea de undă:
\
O Pentru seria Lyman, \(n_1 = 1\).Spectroscopiștii vorbesc adesea despre energie și frecvență ca fiind echivalente. Unitatea cm-1 (wavenumbers) este deosebit de convenabilă. Putem converti răspunsul din partea A În cm-1.,această linie de emisie se numește Lyman alpha și este cea mai puternică linie de emisie atomică de la soare și conduce chimia atmosferei superioare a tuturor planetelor care produc ioni prin îndepărtarea electronilor de la atomi și molecule. Este complet absorbit de oxigen în stratosfera superioară, disociind moleculele O2 la atomii O care reacționează cu alte molecule O2 pentru a forma ozonul stratosferic
B această lungime de undă se află în regiunea ultravioletă a spectrului.,
Exercise \(\PageIndex{1}\): Seria Pfund
seria Pfund de linii din spectrul de emisie al hidrogenului corespunde tranzițiilor de la stări excitate superioare la \(n_1 = 5\). Calculați lungimea de undă a celei de-a doua linii din seria Pfund la trei cifre semnificative. În ce regiune a spectrului se află?
răspuns
\(4.65 \ ori 10^3\, nm\); infraroșu
discuția de mai sus prezintă doar o descriere fenomenologică a liniilor de emisie de hidrogen și nu reușește să furnizeze o sondă a naturii atomului în sine., În mod evident, un model continuu bazat pe mecanica clasică nu este aplicabil și, după cum demonstrează următoarea secțiune, poate fi formulată o legătură simplă între Spectre și structura atomică.
