Introducere în grupa carbonil
în chimia organică, grupa carbonil este o grupă funcțională în care atomul de carbon și oxigen sunt conectate printr-o legătură dublă. Compușii conțin grupare carbonil sunt cunoscute sub numele de compuși carbonil. Grupa carbonil se referă la un monoxid de carbon poate, de asemenea, atașat la un atom anorganic ca un ligand care se numește metal carbonil, de exemplu nichel carbonil.,
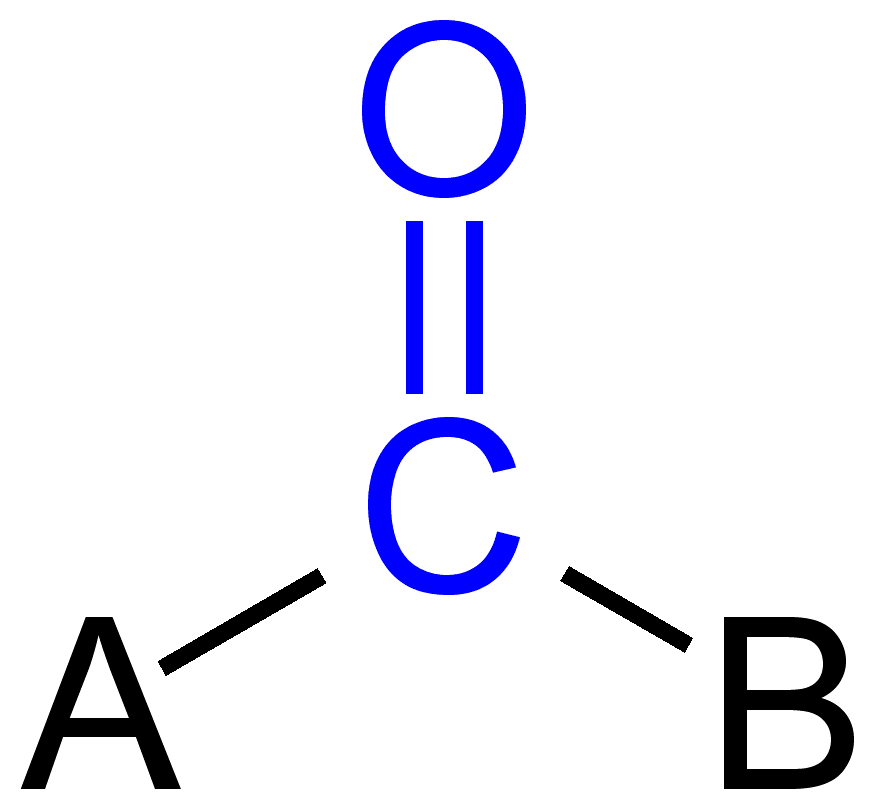
Un grupările carbonil
legătură Dublă în grupa carbonil
de carbon și atomul de oxigen din grupa carbonil sunt în mod normal hibridizat sp2 și, astfel, plannar. Datorită prezenței oxigenului ca atom electronegativ, legătura dublă în grupa carbonil este diferită de legătura dublă în alchene în ceea ce privește reactivitatea. Datorită electronegativității și prezenței a două perechi de electroni, oxigenul devine sarcină parțial negativă, în timp ce carbonul carbonil generează sarcină parțial pozitivă și astfel se observă polaritatea.,din cauza prezenței oxigenului ca atom electronegativ, gruparea carbonil prezintă structura de rezonanță. Structura de rezonanță a grupării carbonil afectează reactivitatea compusului. Atomul de oxigen mai electronegativ atrage electronul din Centrul de carbon face carbonul carbonil parțial electropozitiv și oxigenul parțial electronegativ. Astfel polaritatea generează în compusul carbonil.
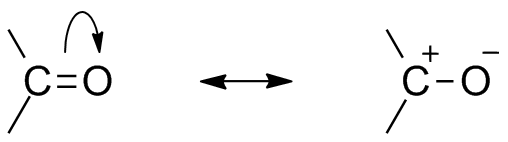
Acest electropositive carbonil de carbon sau electrofil poate fi acum atacat de un nucleofil.,
Reactivitate
Carbonil Alchilare
Alchilare de grupa carbonil de nucleofil plus de reacție cu ajutorul reactivului Grignard sunt afișate după cum urmează:

proprietăți Fizice de compuși carbonilici
- punctul De fierbere ale aldehidelor și cetonelor sunt mai mari decât punctul de fierbere al eteri și alcani al similare masă moleculară.
- din nou, punctul de fierbere al aldehidelor și cetonelor este mai mic decât alcoolii corespunzători.,multe aldehide superioare au miros plăcut și utilizate în parfumuri sau ca aromă artificială, în timp ce membrul inferior al seriei lor omoloage au miros înțepător.
- cetonele superioare au miros bland și mai mici au miros plăcut, cum ar fi acetona.
- aldehidele mici și cetonele sunt solubile în apă, dar pe măsură ce lungimea lanțului crește, solubilitatea scade.forțele de dispersie van der Waals devin mai puternice pe măsură ce moleculele devin mai lungi.,
h-bonding în carbonil goup
datorită formării h-bonding între oxigenul carbonil și hidrogenul moleculei de apă, compușii carbonilici inferiori sunt solubili în apă. Dar, pe măsură ce lanțul crește, vine pe calea formării legăturii de hidrogen și solubilitatea scade.din cauza polarității în grupa carbonil și prezența forțelor de dispersie va exista o atracție între două molecule din apropiere. Acest lucru face ca punctul de fierbere al compușilor carbonil să fie mai mare decât alcanii corespunzători., În tabelul următor observați că punctul de fierbere al compușilor carbonil sunt mai mari decât alcanii corespunzători și mai mici decât alcoolii.,v>Boiling point (o C)
Spectroscopy
Infrared spectroscopy
The absorption of carbonyl group depends on the geometry of the molecule., De obicei, absorbția luminii infraroșii arată la numărul de unde at aproximativ 1600-1900 cm−1 (5263 nm până la 6250 nm).
Rezonanța Magnetică Nucleară
RMN-ul de carbon al carbonului carbonil arată un vârf aproximativ între 160-220 ppm.
