trifluorură de azot proprietăți chimice,utilizări, producție
descriere
trifluorura de azot este un gaz incolor, cu miros redus. Trifluorura de azot este un oxidant care este apoidinamic stabil, cu excepția temperaturilor ridicate. La temperaturi de până la aproximativ 482°F (250°C), reactivitatea sa este comparabilă cu oxigenul. La temperaturi mai ridicate, reactivitatea sa este similară cu fluorul datorită disocierii apreciabile în NF2 și F-., La thennal disociere de trifluorură de azot a fost studiat de un număr de anchetatori și a fost găsit un vârf în intervalul de temperatură de 1100K la 1500K. În manipularea trifluorurii de azot, condiții ar trebui să fie evitate, care poate duce la temperaturi ridicate, cum ar fi compresie adiabatică de la rapid de presurizare a unui sistem.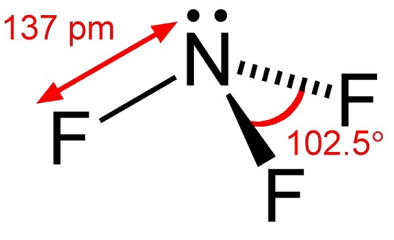
trifluorurii de Azot acționează în principal asupra elementelor ca fluorurarea agent, dar nu foarte activ la temperaturi mai mici., La temperaturi ridicate, trifluorura de azot pirolizează cu multe dintre elemente pentru a produce tetrafluorură de azot și fluorura corespunzătoare. Piroliza trifluorurii de azot peste cornetele de cupru produce tetrafluorură de azot într-un randament de 62% până la 71% la 707°F (375°c). Piroliza peste carbon este mai completă.
proprietăți chimice
trifluorura de azot este un gaz incolor. Miros de mucegai. Livrat ca gaz comprimat nelichefiat.
proprietăți fizice
gaz incolor; miros mucegăit; lichefiază la -128,75°C; densitatea lichidului 3.,116 g/mL; presiune de vapori la -158°C 96 torr; se solidifică la -206.8°C; temperatura critică -39.15°C; presiune critică 44.02 atm; volum critic 126 cm3/mol; foarte puțin solubilă în apă.
utilizează
trifluorura de azot este un agent de curățare etchant și de cameră.
oxidant pentru combustibili de mare energie, sinteză chimică.
utilizează
trifluorura de azot este un gaz care este format din atomi de azot și fluor., Industria electronică globală utilizează trifluorură de azot în procesele sale de curățare, deoarece gazul depășește alte alternative, este mai ușor și mai sigur de manevrat și ajută la reducerea emisiilor de gaze cu efect de seră.
producătorii de semiconductori, celule solare cu film subțire și afișaje cu ecran plat folosesc trifluorură de azot pentru curățarea camerelor de proces. În interiorul camerelor, straturi subțiri de filme semiconductoare și izolatoare sunt aplicate pe plachete și panouri., Trifluorura de azot îndepărtează reziduurile pe care aceste filme le lasă pe pereții camerei, astfel încât camerele să poată funcționa eficient și să producă un dispozitiv de calitate.
trifluorura de azot oferă multe beneficii față de agenții de curățare alternativi. Este stabil la temperatura camerei, deci este relativ ușor și sigur de manevrat. De asemenea, este ușor de utilizat trifluorura de azot pentru a forma un gaz energetic sau reactiv sau o plasmă—un gaz cu electroni liberi. Durata de viață relativ lungă a radicalilor de fluor produși în plasmă face din trifluorura de azot un agent de curățare eficient.,
utilizări
trifluorura de azot a fost utilizată cu succes în cantități mari ca sursă de fluor pentru laserele chimice de mare energie. Este preferat overfluorine datorită ușurinței sale comparative de manipulare în condiții ambientale.
Recent, o creștere a cantității de nitrogentrifluoride este utilizat în semiconductorindustry ca un uscat persoană, arată significantlyhigher etch prețurile și selectivități în comparație cu carbon tetrafluoride și amestecuri carbonului tetrafluoride și oxigen.,
trifluorurii de Azot a fost, de asemenea, folosit ca oxidant în rachete, la începutul anilor 1960, dar thisapplication nu a fost comercializat.
de Pregătire
trifluorurii de Azot se prepară prin electroliza fie topit fluorură de amoniu, NH4F, sau s-a topit de amoniu, acid florhidric, NH4HF2 (sau fluorură de amoniu în anhidru HF). În timp ce NH4F metodă este de preferat, deoarece formele de azot trifluorură ca singurul produs, electroliza de amoniu acid fluor produce o cantitate mică de diazot difluorura, N2F2,și NF3.,
De asemenea, trifluorura de azot poate fi preparată prin reacția amoniacului cu fluor diluat cu azot într-un reactor ambalat cu cupru. Alte azot fluoruri, cum ar fi N2F2, N2F4, și NHF2, de asemenea, sunt produse. Randamentul produsului major depinde de raportul fluor / amoniac și de alte condiții.
metode de producție
trifluorura de azot poate fi formată dintr-o mare varietate de reacții chimice. Procesul comercial de producție implică fluorurarea directă a amoniacului cu gaz de fluor în prezența luiflorură de amoniu.,
reacții
hidrogenul reacționează cu trifluorura de azot cu eliberarea rapidă a unor cantități mari de căldură și este baza pentru utilizarea trifluorurii de azot în laserele chimice de înaltă energie. Intervalul de inflamabilitate pentru amestecurile trifluorură de azot-hidrogen este de 9,4% mol până la 95% mol trifluorură de azot. Trifluorura de azot reacționează cu compușii organici, dar, în general, este necesară o temperatură ridicată pentru a iniția reacția., În aceste condiții, reacția se va desfășura adesea exploziv și trebuie acordată o mare atenție expunerii trifluorurii de azot la compușii organici. Prin urmare, trifluorura de azot a găsit puțină utilizare ca agent de fluorurare pentru compușii organici.
descriere generală
un gaz incolor cu miros mucegăit. Foarte toxic prin inhalare. Puțin solubil în apă. Coroziv pentru țesut. Sub expunerea prelungită la foc sau căldură containerele se pot rupe violent și rachete. Folosit pentru a face alte substanțe chimice și ca o componentă a combustibililor de rachete.,
aer & reacții de apă
ușor solubil în apă.
profilul de reactivitate
trifluorura de azot este un agent oxidant foarte puternic. Prezintă pericol de incendiu periculos în prezența agenților reducători. Gravează sticla în prezența umidității. Emite vapori toxici și corozivi de fluor atunci când este încălzit până la descompunere . Poate reacționa violent cu hidrogen, amoniac, monoxid de carbon, diboran, hidrogen sulfurat, metan, tetrafluorohidrazină, cărbune. Reacție explozivă cu dioxid de clor., O explozie severă poate apărea atunci când este expusă agenților reducători sub presiune .
pericol
pericol sever de explozie. Coroziv pentru țesut. Methemoglobinemia, afectarea ficatului și a rinichilor.
pericol pentru sănătate
inhalarea trifluorurii de azot poate reduce capacitatea globulelor roșii de a transporta oxigenul. Acest lucru provoacă cianoză sau o decolorare albăstruie a pielii. Respirația trifluorură de azot poate duce, de asemenea, la dureri de cap, amețeli, slăbiciune și confuzie., După expunerea prelungită la concentrații mari, descompunerea globulelor roșii și modificări ale ficatului, rinichilor, splinei și mușchiului cardiac pot apărea ca efecte secundare. În aerul proaspăt, modificările inițiale ale globulelor roșii se vor clarifica pe parcursul mai multor ore, dar persoana trebuie monitorizată în continuare pentru efecte secundare.
pericol de incendiu
substanța nu arde, ci va susține arderea. Unii pot reacționa exploziv cu combustibilii. Poate aprinde combustibilii (lemn, hârtie, ulei, îmbrăcăminte etc.).). Vaporii din gazul lichefiat sunt inițial mai grei decât aerul și se răspândesc de-a lungul solului., Scurgerea poate crea pericol de incendiu sau explozie. Containerele pot exploda atunci când sunt încălzite. Cilindrii rupți pot exploda.
utilizări industriale
trifluorura de azot a fost utilizată cu succes în cantități mari ca sursă de fluor pentru laserele chimice de mare energie. Este preferat față de fluor datorită ușurinței sale comparative de manipulare în condiții ambientale.,
recent, o cantitate tot mai mare de trifluorură de azot este utilizată în industria semiconductorilor ca etchant uscat, prezentând rate și selectivități semnificativ mai mari în comparație cu tetrafluorura de carbon și amestecurile de tetrafluorură de carbon și oxigen.
trifluorura de azot a fost folosită și ca oxidant în rachete la începutul anilor 1960, dar această aplicație nu a fost comercializată.
materiale utilizează
la temperaturi mai mici de 482°F (250°C), trifluorura de azot are o reactivitate similară cu cea a oxigenului și este relativ inertă pentru majoritatea materialelor de construcție., La temperaturi ambientale, alamă,aluminiu, cupru, oțel și oțeluri inoxidabile pot fi utilizate deoarece ratele de coroziune sunt mai mici de 0,1 mil/an. la 160 ° F (71,1°C) au fost determinatepentru aceste materiale. Trifluorurii de azot este alsocompatible cu gaze fluorurate cu materiale, cum ar asTeflon la temperaturi ale mediului ambiant.La temperaturi ridicate și presiuni, trifluorurii de azot este reactivitatea crește tot mai mult, ca de fluor, cu nichel andMonel fiind de preferat materiale de constructii.
profil de siguranță
o otravă. Ușor toxicprin inhalare., Absorbția prelungită poateprovoca mottling de dinți, modificări scheletice.Severe cu pericol de explozie prin chemicalreaction cu agenți de reducere, particularlywhen sub presiune. Un foc de artificii foarte periculos; un oxidant foarte puternic; altfeleinert la temperaturi și presiuni normale.
Expunerea Potențială
Acest material a fost folosit în chemicalsynthesis și ca oxidant pentru înaltă energie combustibili (asan oxidant în rachetă combinații).
efecte fiziologice
ACGIH recomandă o valoare limită limită medie ponderată (TLV-TWA) de 10ppm (29 mgim3) pentru trifluorura de azot., TheTLV – TWA este momentul concentrația medie ponderată pentru o nonnal 8 ore de munca si a40 ore lucratoare, la care aproape toate workersmay fi expuse în mod repetat, zi după zi, fără efecte adverse.
OSHA listează o limită de expunere medie ponderată în timp de 8 ore (TWA-PEL)de 10 ppm (29 mg/m3) pentru trifluorura de azot.TWA-PEL este limita de expunere care nu trebuie depășită de intervalul de 8 ore în fiecare tură de lucru de 8 ore dintr-o săptămână de lucru de 40 de ore.,
toxicitatea de trifluorură de azot este raportate de capacitatea acesteia de a fonn methemoglobina, modificat fonn de hemoglobina incapabil de oxygentransport, și de a distruge celulele roșii din sânge(hemoliză). La încetarea expunerii, methemoglobina revine spontan la hemoglobină. Cu toate acestea, la niveluri ridicate de expunere,poate fi necesară intervenția terapeutică (oxigen, albastru de metilen, transfuzie de schimb). Apariția hemolizei necesită o monitorizare atentă a gradului de anemie și a potențialului de afectare a funcției renale.,
valoarea TLV-TWA a trifluorurii de azot de 10 ppm a rezultat dintr-un studiu care a expus șobolanii la 100 ppm timp de 7 ore pe zi, 5 zile pe săptămână timp de 18 luni. Nu au fost detectate modificări în comportamentele animalelor, ratele inimii sau plămânilor, nivelurile de sânge sau apariția fluorozei. ACGIH a stabilit TLV-TWA la nivelul III 0 al testului.
trifluorura de azot gazos este considerată inofensivă pentru piele și un iritant minor pentruochii și membranele mucoase.
depozitare
buteliile de trifluorură de azot trebuie sprijinite în siguranță în timpul utilizării pentru a preveni deplasarea și încordarea conexiunilor., Buteliile complete trebuie depozitate într-o zonă bine ventilată, protejată de căldură excesivă (125°F sau 51,7°c), situată departe de materiale organice sau inflamabile și securizată. Capacele de protecție a supapei și capacele de evacuare a supapei trebuie să fie fixate în siguranță în orice moment când cilindrul nu este utilizat.
transport
trifluorură de azot UN2451, clasa de pericol: 2.2; etichete: 2.2-gaz comprimat neinflamabil; 5.1-oxidant.Cilindrii trebuie transportați într-o poziție verticală sigură,într-un camion bine ventilat. Protejați cilindrul și eticheteledeteriorarea fizică., Proprietarul de gaz comprimat cylinderis singura entitate permis prin lege federală (49CFR) totransport și le umple. Este o încălcare a transportuluireglementări pentru reumplerea buteliilor de gaz comprimat fărăexprima permisiunea scrisă a proprietarului.
evaluarea Toxicității
toxicitatea de trifluorură de azot este legat de capacitatea acesteia de a fonn methemoglobina, modificat fonn de hemoglobina incapabil de transport de oxigen, și de a distruge celulele roșii din sânge (hemoliză). La încetarea expunerii, methemoglobina revine spontan la hemoglobină., Cu toate acestea, la niveluri ridicate de expunere, poate fi necesară intervenția terapeutică (oxigen, albastru de metilen, transfuzie de schimb). Apariția hemolizei necesită o monitorizare atentă a gradului de anemie și a potențialului de afectare a funcției renale.
incompatibilități
gazul este un oxidant puternic. Prezentepericol periculos de incendiu în prezența agenților reducători. Gravează sticla în prezența umidității., Reacționează withoil, grăsimi, agenți de reducere și alte oxidabil materiale;combustibili, materii organice, amoniac, monoxid de carbon; metan,hidrogen, hidrogen sulfurat; cărbune activat; diborane,apă. Poate reacționa violent cu hidrogen,amoniac, monoxid de carbon, diboran, hidrogen sulfurat, metan,tetrafluorohidrazină, cărbune. Trifluorura de azot vacrește intensitatea unui incendiu existent.
eliminarea deșeurilor
returnați buteliile de gaz compresate reîncărcabile către furnizor., Aerisire în volum mare de concentratedreducing agent (bisulfites, săruri feroase sau hipo)soluție, apoi se neutralizează și culoare pentru canalizare cu largevolumes de apă.
grade disponibile
trifluorura de azot este disponibilă în grade cuprinse între 98% și 99,995% v/vpuritate minimă.
