Cuál es la definición de indicador en química
indicador
Los indicadores son sustancias que muestran un cambio de color cuando entran en contacto con ácidos y bases.el indicador más común utilizado en el laboratorio es el tornasol. Se extrae de líquenes y está disponible en forma de soluciones o en forma de tiras de papel conocidas como papel de tornasol. El papel de tornasol es de color rojo o azul. Cambia de color dependiendo de si el compuesto es un ácido o una base., El papel tornasol azul se vuelve rojo en condiciones ácidas, y el papel tornasol rojo se vuelve azul en condiciones básicas.las soluciones que no muestran cambio de color en ninguno de los indicadores no son ni ácidas ni básicas. Estas sustancias, como ya saben, se llaman sustancias neutrales. Algunos ejemplos de sustancias neutras son el agua, el cloruro de sodio,el azúcar, etc.el tornasol, la naranja de metilo y la fenolftaleína son algunos de los indicadores ácido-base más utilizados que cambian de color de la siguiente manera.,td>
Methyl orange
Phenolphthalein
Litmus : It is a natural dye made from small plants called lichens., Las soluciones de tornasol azul y rojo se preparan a partir de dos variedades diferentes de líquenes.papel tornasol: el papel tornasol azul o rojo se prepara sumergiendo una tira de papel de filtro en soluciones de tornasol azul o rojo. El papel se retira de la solución y se seca.el papel tornasol azul se vuelve rojo en una solución ácida y el papel tornasol rojo azul en una solución básica.fenolftaleína: es un compuesto incoloro. Una solución alcohólica de fenolftaleína se utiliza como indicador., Es incoloro en una solución ácida, pero se vuelve rosado (rojo) en la solución básica:
Naranja de metilo : una cantidad muy pequeña de naranja de metilo sólido se disuelve en agua caliente y se filtra. El filtrado se utiliza como indicador. Se vuelve rojo en soluciones ácidas y amarillo en soluciones básicas.
indicadores universales
Los ácidos o bases pueden ser fuertes o débiles. Los científicos han hecho que sea muy fácil conocer la fuerza de un ácido o una base. Se han dado diferentes concentraciones lo que se conoce como un número de pH que varía de 1 a 14., Uno es considerado como fuertemente ácido y 14, fuertemente básico; 7 es neutro. Puede medir el pH de una solución utilizando ácidos o bases que pueden ser fuertes o débiles. Los científicos han hecho que sea muy fácil conocer la fuerza de un ácido o una base. Se han dado diferentes concentraciones lo que se conoce como un número de pH que varía de 1 a 14. Uno es considerado como fuertemente ácido y 14, fuertemente básico; 7 es neutro. Puede medir el pH de una solución utilizando un indicador universal.
un indicador universal es una mezcla de indicadores elegidos de manera que da un color diferente para diferentes valores de pH., El indicador se puede utilizar como líquido o se puede empapar en papel. Este papel se llama papel pH.
Cuando un papel pH se sumerge en un ácido o una base, el color obtenido se puede comparar con la tabla que se muestra a continuación.

indicadores naturales:
algunos indicadores naturales útiles se discuten a continuación.(i) jugo de cúrcuma es de color amarillo. Permanece amarillo en soluciones ácidas o neutras, pero se vuelve marrón oscuro en una solución básica.
(ii) El jugo de col roja en sí mismo de color púrpura, se vuelve rojo en una solución ácida, pero Verde en una solución básica.,
Las soluciones indicadoras se pueden preparar hirviendo partes coloreadas de la planta, como pétalos, en agua durante algún tiempo y colando la parte de la planta. Esta solución da un color diferente en soluciones ácidas y básicas.
por ejemplo, el jugo de col roja cambiará a rojo intenso con ácidos, a púrpura con neutros y a verde y amarillo con bases. El jugo de cebolla también muestra cambios de color similares. Puede poner directamente algunos pétalos de rosa en un plato que contenga vinagre o jugo de limón y algunos pétalos en solución de jabón y ver la diferencia de color.,
Los indicadores domésticos se pueden utilizar para probar si algunas de las sustancias de uso diario enumeradas a continuación son ácidas o básicas.,»d4ee238131″>Vitamine C tablets
(ascorbic acid)
Lemon juice
Orange juice
Tomato juice
Vinegar
Antacids
Toothpaste
Soap solution
Washing soda solutions
Olfactory indicators :
There are substances like onion juice, vanilla essence and clove oil which by change of their smell indicate whether the sample solution is acidic or basic., Estos se llaman Indicadores olfativos.usted ha aprendido que en las reacciones de neutralización un ácido y una base reaccionan para producir sal y agua. Por ejemplo, la reacción de neutralización entre NaOH y HCl da la sal NaCl y el agua.
NaOH + HCl → NaCl + H2O
Por lo tanto, una sal puede definirse de la siguiente manera.una sal es un compuesto formado por la reacción de un ácido con una base en la que el hidrógeno del ácido es reemplazado por el metal.en los ácidos polibásicos, más de un átomo de hidrógeno está presente en una molécula. Estos átomos de hidrógeno pueden ser reemplazados parcial o completamente., Por lo tanto, dos tipos de sales son posibles.
(I)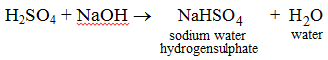
Aquí, el reemplazo parcial de átomos de hidrógeno de H2SO4 ha dado lugar a la formación de hidrogensulfato de sodio.
(ii)![]()
Aquí, el reemplazo completo de átomos de hidrógeno de H2SO4 ha dado lugar a la formación de sulfato de sodio. NaHSO4 y Na2SO4 representan dos tipos de sales.
actividad
Objetivo: ver el efecto de un indicador natural
Materiales necesarios: polvo de cúrcuma, alcohol / agua, solución de jabón y método de vaso de precipitados: –
1., Mezcle 1/4 cucharadita de cúrcuma (haldi) en polvo en 1/4 taza de alcohol en un vaso pequeño. También se puede mezclar con agua, pero la cúrcuma se disuelve mejor en alcohol.
2. Prepare una solución de jabón en otro vaso de precipitados disolviendo un pequeño trozo de jabón de lavar en agua.3. Añadir unas gotas de la solución de cúrcuma-alcohol a la solución de jabón.observación: la solución de jabón se vuelve roja.conclusión: el jabón es una base, y el compuesto (llamado curcumina) que le da a la cúrcuma su color amarillo reacciona con el jabón (una base) para formar un compuesto rojo.
