D – Ja L – Notaatio Ehdoton Kokoonpano Sokereita Ja Aminohappoja,
Mikä erottaa ”D-Glukoosi” alkaen ”L-Glukoosi” ? Tai D-alanine L-alaninesta?
And what is this D – and L – nomenclature, anyway? Lue:
Sisällysluettelo
- D – ja L – Tarjoaa Nopean Pika Nimeämisestä Enantiomeerit
- Miksi Me Vaivautua Tämän Muinaisen Nimikkeistön?,
- L – Ja D – Järjestelmän Määrittäminen ”Absoluuttinen Määritys”
- Neljä-Hiili-Aldehydi D – ja L – Sokereita (Aldotetroses)
- Viiden Hiilen Aldehydi D – ja L – Sokereita (Aldopentoses)
- Kuusi-Hiili-Aldehydi D – ja L – Sokereita (Aldohexoses)
- Mutta Odota Siellä on Enemmän! (Aminohappoja)
- Yhteenveto: D – ja L – Notaatio Sokereita ja Aminohappoja,
- Muistiinpanot
- (Lisäasetukset) Viitteet ja kirjallisuutta
D – Ja L – Tarjoaa Nopean Pika Nimeämisestä Enantiomeerit
D – ja L – notaatio tarjoaa nopean pika nimeämisestä enantiomeerit.,
d-glukoosi on esimerkiksi L-glukoosin enantiomeeri. Koska L-alaniini on D-alaniinin enantiomeeri.
se on annettu seuraavasti. Jonkin sokerin piirretty Fischer-projektio kaikkein hapettuneen hiilen yläreunassa (eli aldehydi tai ketoni)
- jos OH pohjassa kiraalinen keskus pistettä oikealle, sitä kutsutaan D-
- jos OH pohjassa kiraalinen keskus pistettä vasemmalle, sitä kutsutaan L- .
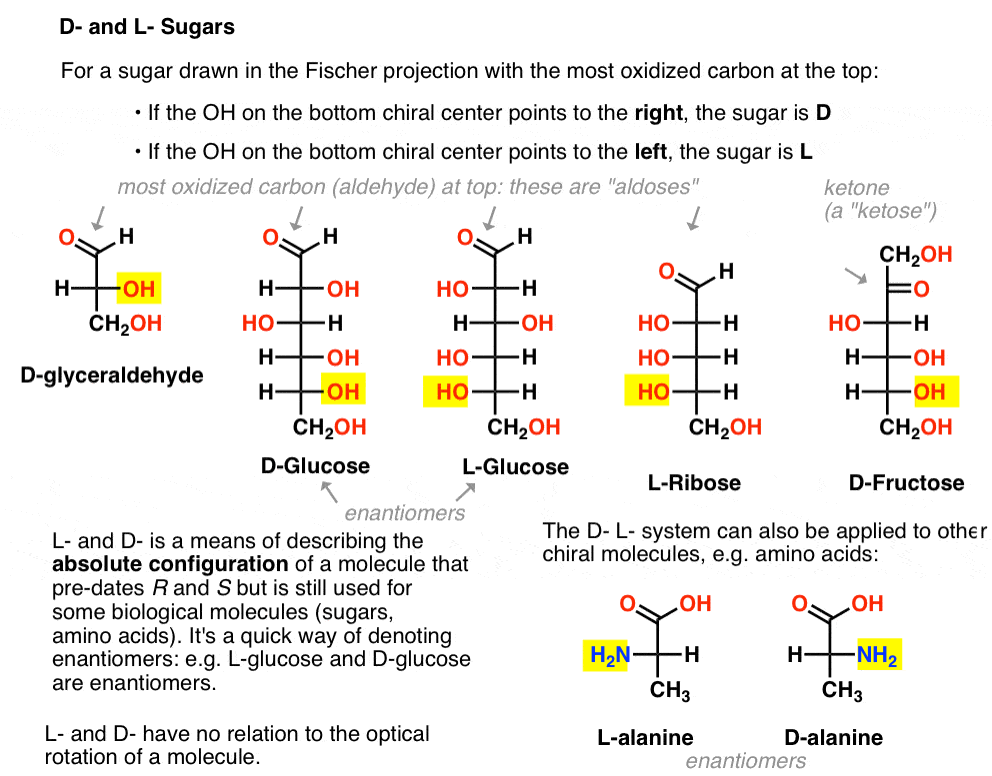
Tämä terminologia voidaan soveltaa myös aminohappoja: ks. L – ja D – alaniini kuvassa yllä.,
2. Miksi Me Vaivaudumme Tähän Muinaiseen Nimikkeistöön?
saatat perustellusti kysyä: eikö meillä ole jo järjestelmä absoluuttisen kokoonpanon määrittämiseen ? Miksi tarvitsemme uuden järjestelmän?
D-L järjestelmä ei ole uusi järjestelmä, ihmiset. Se on vanha järjestelmä – se on vanhempi Cahn-Ingold-Prelog.
D-L-järjestelmä on kirjaimellisesti jäänne hevosen ja buginen aikakausi, vuodelta Emil Fischerin työtä hiilihydraatteja 1800-luvun lopulla – kun orgaaniset kemistit ei ollut tapa määrittää absoluuttinen konfiguraatio stereocenters, joka tuli mahdolliseksi vasta vuonna 1951 (thx, Bijvoet).,
joten miksi sitä vielä käytetään? Eikö se pitäisi lähettää historian roskiin, liukumäkisääntöjen, 8-raitaisten kasettien ja 5 ¼ ” levykkeiden kanssa?
hyvin, on kukoistavia yhteisöjä osissa maaseutu-Amerikkaa, jossa hevoskärryt jatkuvat – jos tietää, mistä etsiä. (Ehkä joskus tulee kommuuneja, joissa ihmiset käyttävät vain 1970-ja 1980-lukujen tietotekniikkaa?)
samoin on olemassa orgaanisen kemian tasku, jossa D-L-järjestelmä löytää yhä käyttöä, ja se on nimenomaan sokerien ja aminohappojen valtakunnassa.,
Tämä ei muuten ole amissien kemistien kapina CIP-järjestelmän nykyisiä pahuuksia vastaan. Siellä on ainakin 3 hyvää syytä, tässä tapauksessa sokereita ja aminohappoja, käyttämällä L – ja D- :
- Lyhyys. D-glukoosi on paljon nopeampi kirjoittaa ja sanoa, kuin (2R,3S,4R,5R)2,3,4,5,6-pentahydroxyhexanal. L/D – järjestelmä mahdollistaa kokoonpano molekyyli, jossa on useita kiraaliset keskukset voidaan tiivistää yhdellä kirjaimella (plus sen yleinen nimi, tietenkin – kiitos Noel muistutuksesta)
- Enemmän lyhyys., Se sattuu olemaan nopea tapa viitata enantiomeerit. L-glukoosin enantiomeeri on D-glukoosi. L-tryptofaanin enantiomeeri on D-tryptofaani. Ja vaikka voisimme käyttää (+)- tai (–)- etuliitteitä erottaa kaksi enantiomeeria glukoosi ja muut sokerit, merkki optinen kierto voi vaihdella liuotin, lämpötila, pitoisuus -, ja muut tekijät, joka tekee siitä vähemmän kuin ihanteellinen. Plus, L – ja D – viittaavat nimenomaan absoluuttinen kokoonpano, kun taas (kuten totesimme aiemmin) ei ole yksinkertainen suhde merkki optinen kierto ja kokoonpano.,
- on käynyt ilmi, että useimmat luonnossa esiintyvät sokerit ovat D-, ja useimmat luonnossa esiintyvät aminohapot ovat L- . Siellä on valtava määrä tietoa pakattu, että lausunto, ja ei ole kilpailevia järjestelmä (R/S, +/–), joka voisi korvata L – ja D – kanssa yksittäinen merkki. Huomautus
se on toistettava: sokereiden ja aminohappojen kanssa L – ja D – voivat olla hyödyllisiä nimityksiä. Muille molekyyleille sen voi pitkälti unohtaa.
joten mikä on tämä D- / L – järjestelmä, ja miten nämä termit liittyvät rakenteeseen?,
Liity minua kun me matkustaa takaisin ajassa…
L – Ja D – Järjestelmän Määrittäminen ”Absoluuttinen Määritys”
Emil Fischer alkoi opiskella hiilihydraatteja myöhään 1880-luvulla. Se oli tiedossa, että aika kautta (Van ei Hoff), että hiili oli tetraedri, ja se oli myös tiedossa, että molekyylit sisältävät hiiltä jossa on neljä eri substituentteja voisi kiertää kone-polarisoitunut valo (esim. Pasteur). Mikä ei ollut tiedossa, oli ehdoton kokoonpano tahansa kiraaliset molekyylit – mitä meidän pitäisi viitata tänään heidän ”R” ja ”S” kokoonpanoissa.,
yksinkertaisin kiraalista keskusta sisältävä hiilihydraatti on glyseraldehydi, C3H6O3. Glyseraldehydissä on kolme karbonia, mikä tekee siitä ”trioosin”. Eniten hapettuneen hiilen glyceraldehyde on aldehydi, joka tekee myös ”aldose”.
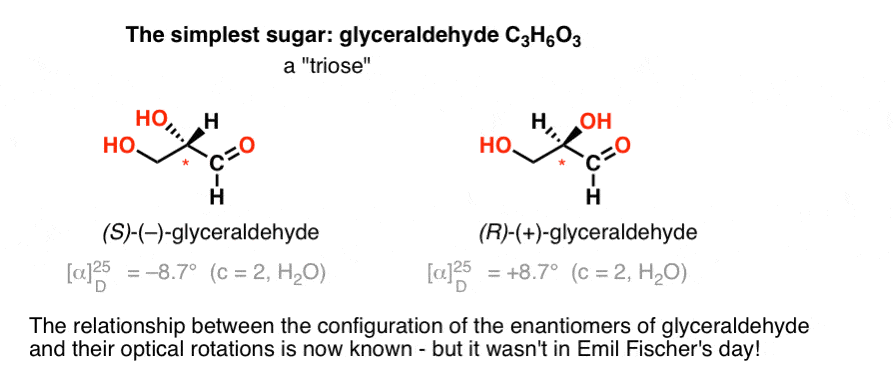
Vuonna 1888, kaksi enantiomeeria ja glyceraldehyde oli eristetty ja ominaista., Mutta koska ei ole yksinkertainen korrelaatio kokoonpano kiraalinen keskus ja mihin suuntaan se pyörii kone-polarisoitunut valo, Emil Fischer ei ollut tapa sitoa takaisin optinen kierto (+)- ja (–)-glyceraldehyde ehdoton kokoonpanosta atomien ympärillä on kiraalinen keskus.
nykyisellä terminologialla hän ei osannut tietää, onko (–)-glyseraldehydi (R) vai (S).
tämän keskeisen tiedon puutteessa Fischer päätti arvata.,
arvaus, joka osoittautui olevan oikea, oli se, että (–)-glyceraldehyde oli kokoonpano me nyt kutsumme S, ja että (+)-glyceraldehyde on kokoonpano me nyt kutsumme R.
tietenkin, Cahn, Ingold, ja Prelog ei ollut vielä syntynyt, ja CIP-järjestelmä olisi vain kehittynyt, kun Bijvoet työ vuonna 1951. Niinpä Fischer kehitti oman nimistönsä.
Piirustus glyceraldehyde mitä myöhemmin kutsutaan Fischer-projektio, hän määritetty kokoonpano vasemmalla (–)-glyceraldehyde, ja kutsui sitä L- (lyhyt latinalaisen laevo )., Sitten hän määritetty kokoonpano oikealla (+)-glyceraldehyde, ja kutsui sitä D- (latinalaisen lääkettä ).
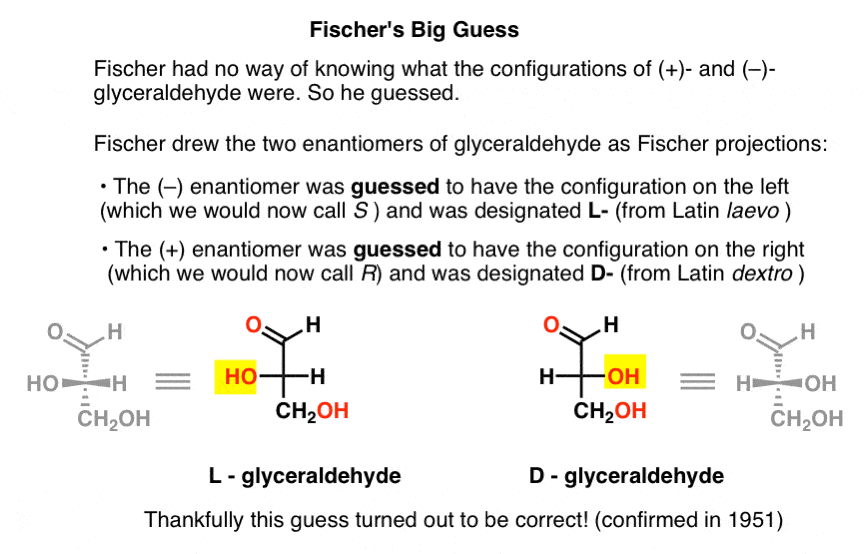
Miksi tämä on niin tärkeää?
Määrittäminen absoluuttinen määritys L – ja D – glyceraldehyde oli vähän kuin osoitetaan Prime Meridian (0° pituutta), Royal Observatory Greenwich, Englannissa., Aivan kuten pituusaste joka toinen paikka maan päällä voi sitten olla määritetty suhteessa, että kohta, jos niiden suhteellinen etäisyydet olivat tiedossa, absoluuttinen kokoonpano joka toinen stereocenter voitaisiin sitten määrittää, jos sen kokoonpano suhteessa L – tai D – glyceraldehyde oli tiedossa.
se ei välttämättä ole selkein vertaus. Katsotaanpa siis 4-hiilisiä sokereita toisesta esimerkistä.,
Neljä Hiili-Aldehydi D – ja L – Sokereita (Aldotetroses)
Kun absoluuttinen kokoonpanoissa L – ja D – glyceraldehyde ehdotettiin, absoluuttinen kokoonpanoissa muita kiraaliset yhdisteet voisi sitten olla perustettu analogisesti (ja paljon kemiallisia murisija työtä).
se ei ole ratkaisevaa tälle päivälle, mutta esimerkkinä tällaisesta päättelystä, katso tämä .
kun käsite kiraaliset keskukset oltiin käyttöön, olet todennäköisesti tietää, että molekyyli n kiraaliset keskukset on 2n stereo (niin kauan kuin ei ole meso-yhdisteet).,
on kaksi nelihiilistä aldoosia, treoosi ja erytrose. Molemmilla on kaksi kiraalista keskusta. Kumpikin on olemassa enantiomeerien parina (L – ja D -), jolloin stereoisomeerejä on yhteensä neljä.
tässä ne ovat. Tärkeä asia huomata alla olevassa kaaviossa on, että L-perheen sokerit on OH-ryhmän pohja kiraalinen hiili vasemmalla, ja D-perhe on OH-ryhmän pohja kiraalinen hiili oikealla (korostettu).,
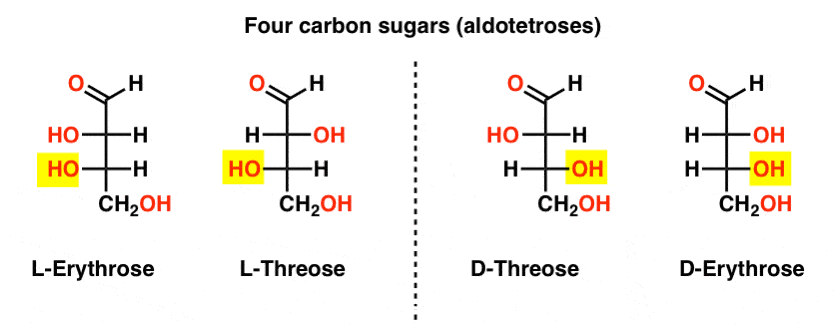
Katso, miten L-Erythrose ja L-Threose rakentaa stereocenter perustettu vuonna L-glyceraldehyde (korostettu), ja D-Erythrose ja D-Threose rakentaa stereocenter perustettu vuonna D-glyceraldehyde (korostettu).
sokerit rakentuvat hieman binäärijärjestelmän tapaan; jokaisen stereocenterin voi ajatella olevan ”bitti”, jolla voi olla jompikumpi kahdesta arvosta. L-erytrosen ja L-treoosin konfiguraatio eroaa vain yhdessä stereosoittimessa. Jos kääntäisimme h: n ja OH: n asentoa, saisimme toisen., Tämä suhde on nimi, että et voi nähdä joskus: kaksi molekyylejä, jotka on päinvastainen kokoonpano vain yksi stereocenter kutsutaan epimers, varsinkin kun atomit kiinnitetty stereocenter on vetyä (H).
Viisi Hiiltä Aldehydi D – ja L – Sokereita (Aldopentoses)
tunnetuin nimi listalla pitäisi olla riboosi, joka on sokeri selkäranka ribonukleiinihappo (RNA).
vasemmalla puolella kaaviossa alla, meillä on L-aldopentoses, jossa kaikki jakavat saman kokoonpanon pohjan stereocenter kun aldehydi on sijoitettu alkuun.,
niiden enantiomeerit, d-aldopentoosit, ovat oikealla puolella, joilla kaikilla on sama pohjistereocenterin konfiguraatio (korostettu).
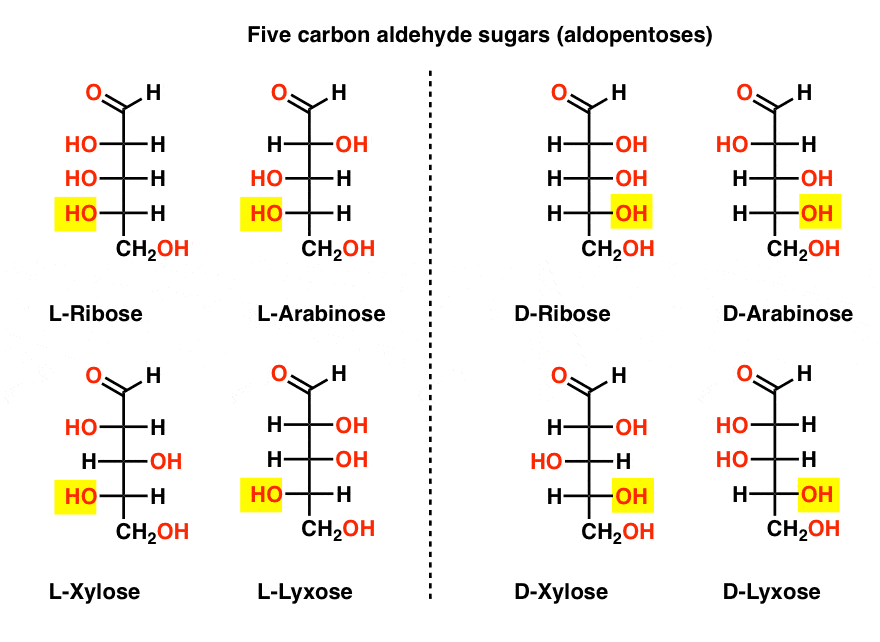
tässä vaiheessa meidän pitäisi huomauttaa, että ylivoimainen enemmistö sokerit Maa-perustuu elämänmuodot ovat D – sokereita, kuten D-riboosi, kuten selkäranka-RNA: ta. Se, miksi ja miten kaikki maan eliöt päätyivät d-sokereihin, on arvoitus, sillä oletetaan, että L-sokerit olisivat toimineet yhtä hyvin.,
Kuuden hiiliatomin Aldehydi D – ja L – Sokereita (Aldohexoses)
– Jos on olemassa 4 aldopentoses, jokainen kuin D – L – pari enantiomeerit (8 stereo yhteensä) niin kuinka monta aldohexoses ovat siellä?
d-L – pareja on 8 (stereoisomeereja yhteensä 16). Tutuin on glukoosi, mutta todennäköisesti tunnistat mannoosin ja galaktoosin. Jotkut ovat harvoin, jos koskaan, löytyy luonnosta (idose, kukaan?).
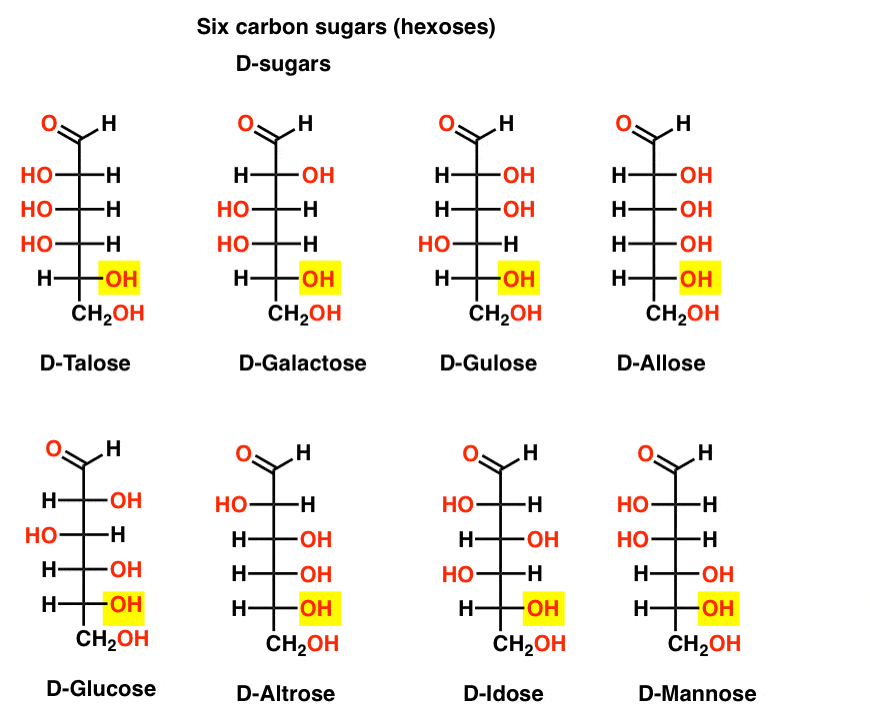
tässä ovat D-aldoheksoosit. Huomaa, miten niillä kaikilla on sama kokoonpano alimmassa kiraalikeskuksessa – sama, jonka näimme d-glyseraldehydissä.,
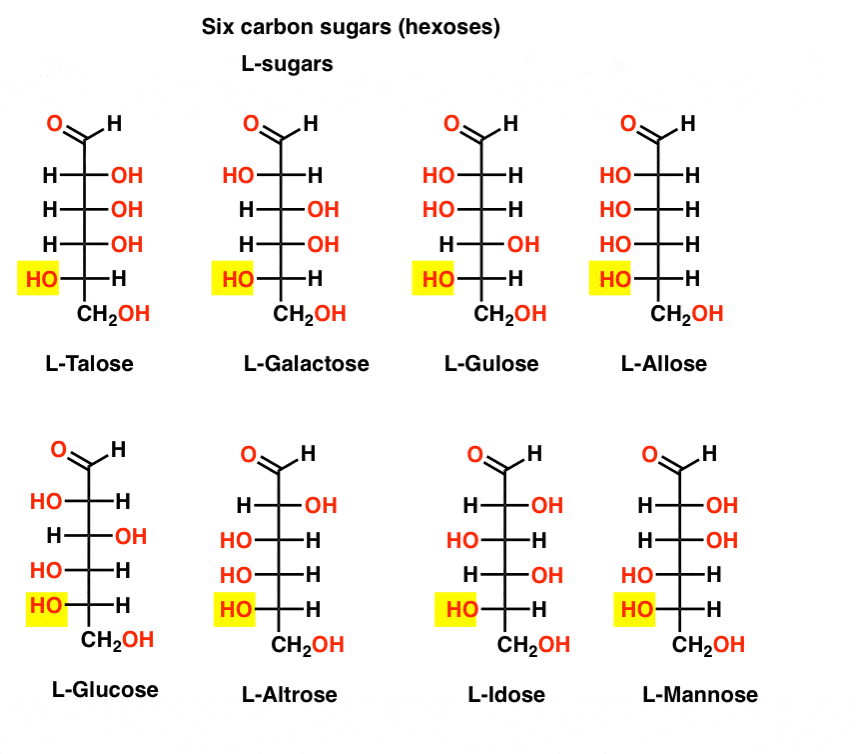
toisin kuin D-sokereita, L – sokereita (alla) ovat harvoin löytyy luonnosta. Mielenkiintoista on, että L-glukoosia on tutkittu sokerin korvikkeena. Sen maku on mahdoton erottaa luontaisesti D-glukoosia, mutta ei tarjoa ravintoa, koska se ei voi olla rikki, meidän (kiraalinen) – entsyymejä. Kuten käy ilmi, tuotanto on aivan liian kallista kilpailla splenda, stevia, aspartame et. al.
OK, se riittää. Seitsemähiilisiä sokereita on tehty (aldoheptoosit), mutta ne eivät ole biologisesti merkittäviä.,
7. Mutta odota-on enemmän! (Aminohappoja)
Jos piirtää aminohappoja Fischer-projektio eniten hapettunut ryhmän alkuun (karboksyylihappo) sitten voit myös määrittää L – ja D-.
19 kiraalinen aminohappoja, jotka on sisällytetty proteiineja (proteinogenic on oikea termi) ovat kaikki L- . (Glysiini on akiraalinen, joten D – ja L – eivät päde). Jotkut D – aminohapot ovat luonnossa esiintyviä, mutta ne ovat harvinaisia (useimmiten esiintyy bakteereissa, lukuun ottamatta vesinokkaeläimen myrkkyä) ja niitä ei koodata mRNA.,
mielenkiintoista on, että vaikka kaikki 19 kiraalista aminohappoa ovat L- , 19: stä vain 18 on (S). Mikä on poikkeus?
(This is good organic chemistry bar trivia).
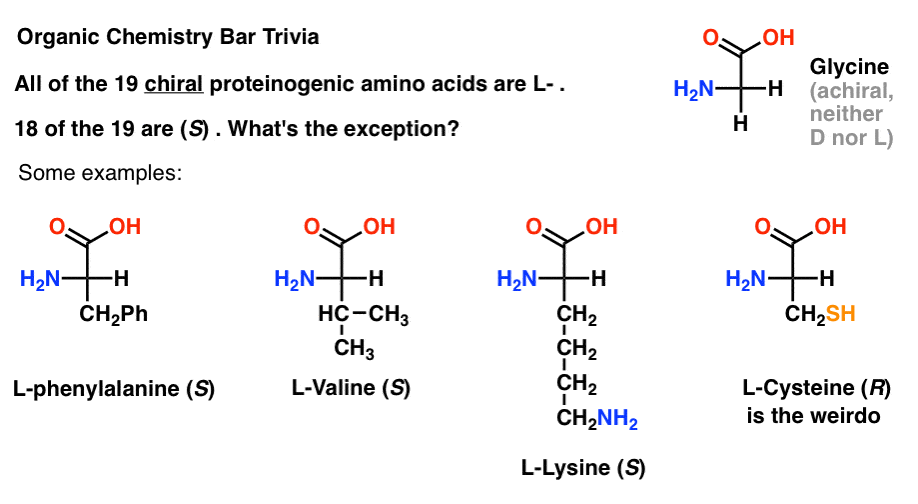
Kysteiini on kummajainen.
(bonuspisteitä, jos sanoit myös selenokysteiini … nörtti).
Yhteenveto: D – ja L – Notaatio Sokereita Ja Aminohappoja,
Niin että on D – L – järjestelmän luovutus ehdoton kokoonpano. Se toimii hyvin sokerit, koska ne voidaan rakentaa niin järjestelmällisesti (kuten binary järjestelmä). Siitä on hyötyä myös aminohapoille., Tärkeintä on vain katsoa alempaa stereocenteria, kun se piirretään Fischerin projektioon. Eikö niin? D. Lähti? L.
sokerit eivät tietenkään aina ole niin auttavasti piirrettyjä Fischerin projektioissa – ne muodostavat renkaita. Kirjoitamme D – ja L-in syklisten sokereiden määrittämisestä tulevaisuudessa.
kaikki mitä minulla on sanottavaa on, kiittää mitä tahansa jumaluutta, jonka päätät uskoa siihen, että Fischerin arvaus osoittautui oikeaksi. Se olisi valtava riesa käydä läpi 70+ vuotta kemian kirjallisuus tietäen, että väärä kokoonpano oli sille kaikki sokerit ja aminohapot.,
Kiitos Thomas Strublen avusta tässä virassa.
huomautukset
Huomautus 1. ”toiseksi viimeinen stereocenter useimmissa kiraalinen sokerit on R, kun taas stereocenter useimmissa aminohappoja on S” ei ole aivan sama rengas, varsinkin kun kysteiini on R. ]
Huom. Tässä on ajatuskoe erytrosen ja treoosin suhteellisten konfiguraatioiden määrittämiseksi., (Sanon ”ajatuskoe”, koska en halua kuulua erityiset reagenssit, jotka voivat olla häiritseviä)
Jos yksi alkaa puhdas (+)-erythrose ja hapettuu ensisijainen alkoholi aldehydi käyttäen tunnettuja menetelmiä, saadaan yhdiste, joilta puuttuu optinen kierto. Sama pätee ( – ) – erytroseen, joka palauttaa täysin identtisen yhdisteen. Tästä voidaan päätellä, että rakenne uusi yhdiste on oltava sellainen, että molekyyli on sisäinen peili kone (eli se on meso). .,
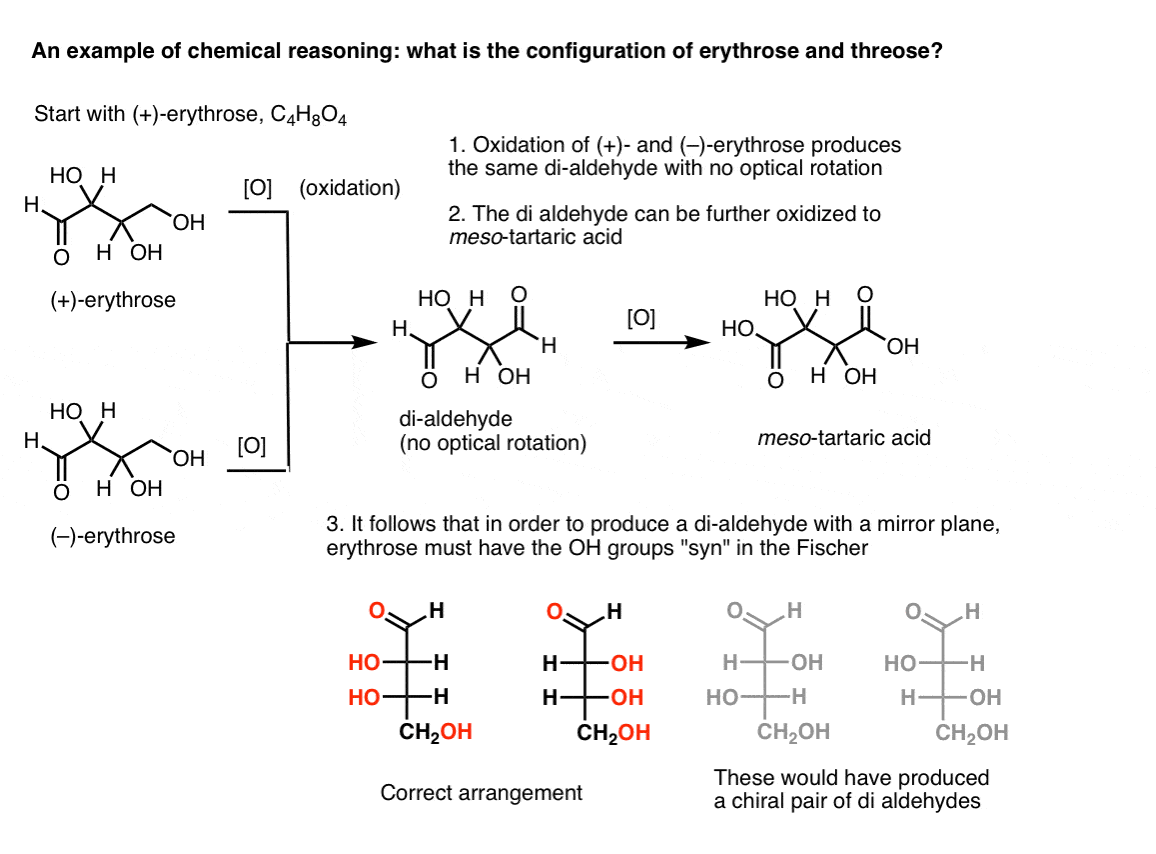
sen sijaan, suorittaa saman operaation (+)-threose johtaa di-aldehydi, joka ylläpitää optinen kierto. Yhdiste, jolla on yhtä suuri ja vastakkainen optinen kierto, muodostuu suorittamalla sama operaatio ( – ) – kolmosilla. Nämä kaksi yhdistettä ovat enantiomeerejä. Jotta tämä olisi totta, hydroksyyliryhmien suhteellisen suuntautumisen kolmioosissa on oltava antia. Nämä yhdisteet voidaan hapettaa edelleen tuottamaan ( – ) – ja ( + ) – viinihappoa.,
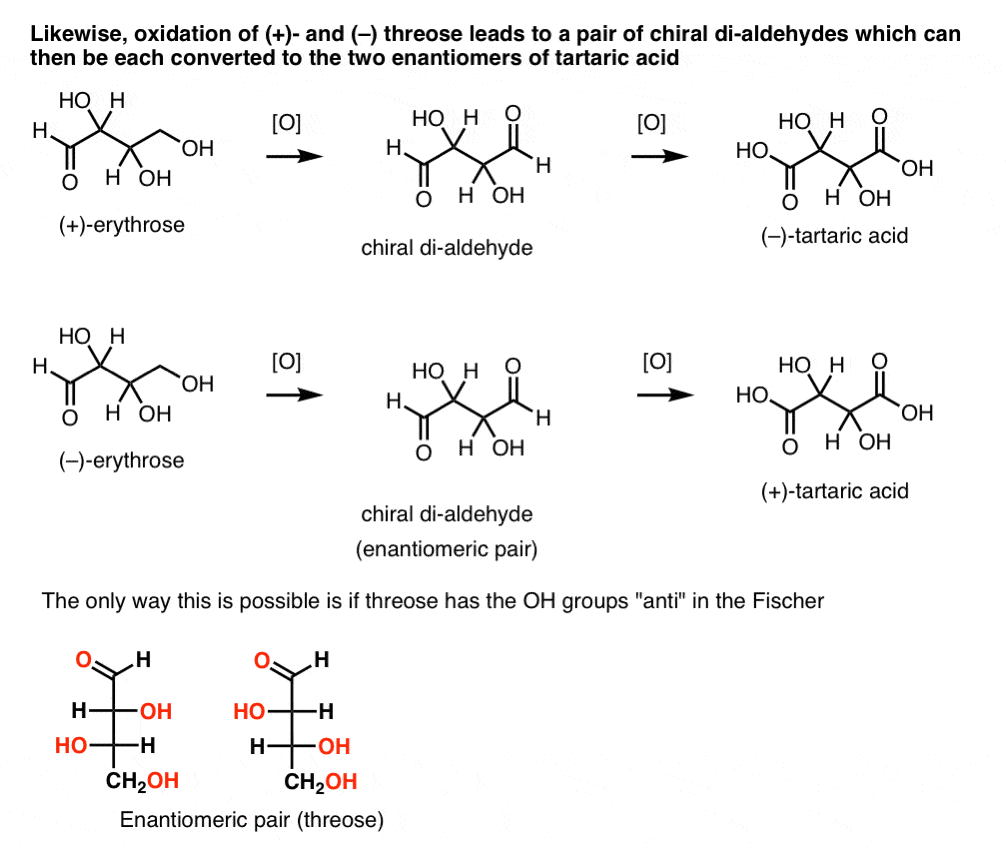
samaa päättelyä voidaan käyttää vastakkaiseen suuntaan (vähennys). Esimerkiksi joko (+)- tai (–)- erythrose voidaan vähentää tetra-ol erytritoli, joka on meso.
Lisäksi, vähennys (+)- ja (–) threose johtaa enantiomeric pari tetra-ols, threitol.
näistä faktoista voidaan päätellä OH-ryhmien suhteellinen suunta.
(Lisäasetukset) Viitteet ja kirjallisuutta
- Über die Bezeichnung von optischen Antipoden durch die Buchstaben d ja l
Emil Fischer
Ber. 1907, 40 (1), 102-106
DOI: 10.,1002 / cber.19070400111
This is the famous paper where Prof. Emil Fischer (mielivaltaisesti!) osoitettu (-) – glyseraldehydi L-stereokemia. - Synteesit vuonna Puriini ja Sokeri Ryhmä
Emil Fischer
Nobel-Luento, 1902Fischerin Nobel-Luento, jossa hän puhuu hänen työnsä ole vain hiilihydraatteja, mutta myös puriinit, jotka yhdisteitä, kuten kofeiinia ja teobromiini ovat jäseniä. Professori Fisher ennustaa energiajuomien (esim., Red Bull), jossa todetaan, ”kun käyttää hieman mielikuvitusta päivä voidaan ennakoida, kun pavut eivät ole enää velvollisia tekemään hyvää kahvia: pieni määrä jauhetta kemiallisten toimii yhdessä veden kanssa antaa suolainen, virkistävä juoma yllättävän halvalla”.
- Määrittäminen Absoluuttinen Konfiguraatio Optisesti Aktiivisia Yhdisteitä avulla X-Säteet
BIJVOET, J., PEERDEMAN, A. & van BOMMEL, A.,
Luonto 1951, 168, 271-272
DOI: 1038/168271a0
kuuluisa paperi, joka todistaa, käyttäen X-ray-rakenteellinen analyysi, että ”Emil Fischer on yleissopimus, joka on määritetty configuration Kuvion. 2 dekstrorotatoriseen happoon, näyttää vastaavan todellisuuteen”. - Emil Fischerin löytö glukoosin kokoonpanosta. Semicentennial jälkikäteen
C. S. Hudson
Journal of Chemical Education 1941, 18 (8), 353
DOI: 10.1021/ed018p353
aikainen tarkastelu, joka kattaa Professori Emil Fischer työtä hiilihydraattien kemiaa., - Emil Fischer on Todiste Kokoonpano Sokereita: A Centennial Kunnianosoitus
Frieder W. Lichtenthaler
Angew. Kem. Int. Toim. 1992, 31 (12), 1541-1556
DOI: 10.1002/anie.199215413
erittäin luettava arvostelu vuodelta 1992, joka kattaa Professori Fischerin työtä hiilihydraattien kemia ja menee syvällistä osaksi stereochemical tehtäviä hiilihydraatteja.
