Johdanto karbonyyliryhmä
orgaaninen kemia, karbonyyli-ryhmä on toiminnallinen ryhmä, jossa hiili-ja happiatomi ovat yhteydessä kaksoissidos. Yhdisteet sisältävät karbonyyliryhmän tunnetaan karbonyyliyhdisteinä. Karbonyyliryhmä viittaa hiilimonoksidiin, joka voi myös kiinnittyä epäorgaaniseen atomiin ligandina, jota kutsutaan metallikarbonyyliksi, esimerkiksi nikkelikarbonyyliksi.,
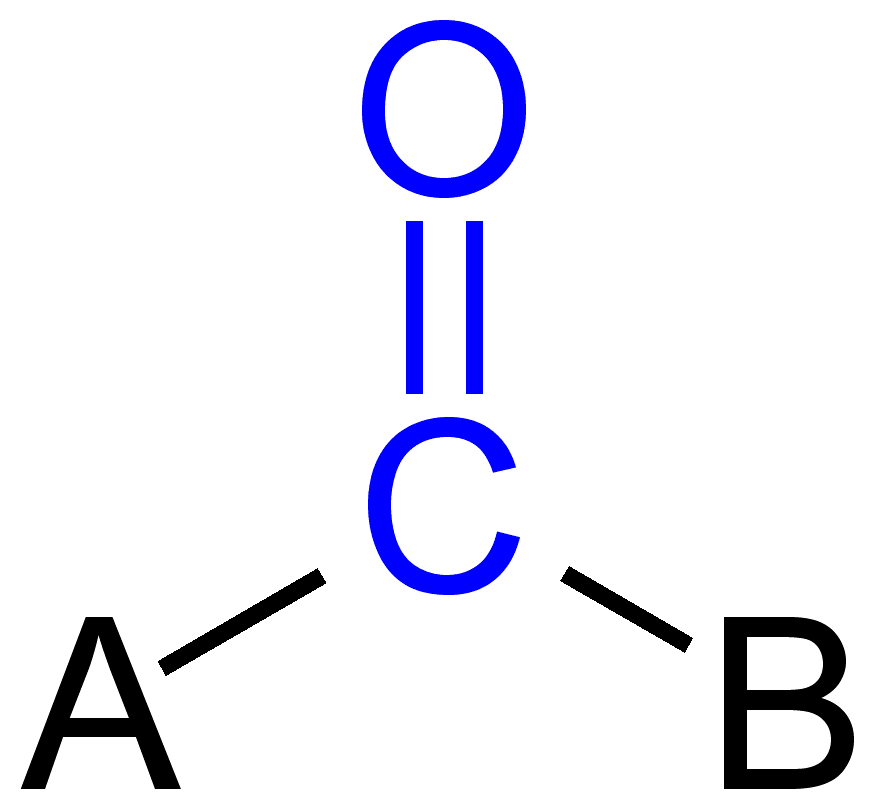
Jotkut karbonyyli ryhmät
kaksoissidos karbonyyliryhmä
hiilen ja hapen atomin karbonyyliryhmä ovat yleensä sp2 hybridisoitiin ja siten plannar. Koska hapen läsnä ollessa kuin electronegative atomin, double bond karbonyyliryhmä on erilainen kuin kaksoissidos alkeenit kannalta reaktiivisuus. Koska enemmän elektronegatiivisuus ja läsnäolo kaksi lone-pair-elektronit, happi tulee osittain negatiivinen varaus, kun karbonyyli hiili tuottaa osittain positiivinen varaus, ja siten, että napaisuus on havaittu.,
Karbonyyli resonanssi rakenne
Koska hapen läsnä ollessa kuin electronegative atomin, karbonyyli-ryhmä esittää resonanssi rakenne. Karbonyyliryhmän resonanssirakenne vaikuttaa yhdisteen reaktiivisuuteen. Enemmän electronegative happiatomi vetää pois electron hiilestä keskus tekee karbonyyli hiili osittain electropositive ja hapen osittain electronegative. Näin napaisuus syntyy karbonyyliyhdisteen sisällä.
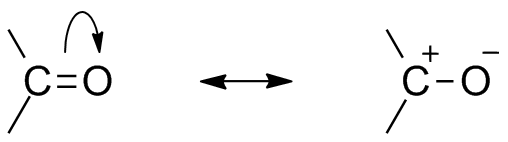
Tämä electropositive karbonyyli hiili-tai electrophile voi nyt olla hyökkäsi nucleophile.,
Reaktiivisuus
Karbonyyli-Alkylointi
Alkylointi ja karbonyyli-ryhmän nukleofiiliset lisäksi reaktio käyttämällä Grignardin reagenssin näkyvät seuraavasti:

Fysikaaliset ominaisuudet karbonyyli-yhdisteiden
- kiehumispiste aldehydit ja ketonit on korkeampi kuin kiehumispiste eetterit ja alkaanit samanlaisia molekyylimassa.
- taas aldehydien ja ketonien kiehumispiste on pienempi kuin vastaavat Alkoholit.,
- Paljon suurempi aldehydejä on miellyttävä tuoksu, ja käytetään hajusteita tai keinotekoisia aromeja, kun taas pienempi niiden homologinen sarja on pistävä haju.
- korkeammilla ketoneilla on mitäänsanomaton haju ja matalammilla miellyttävä haju, kuten asetoni.
- Pienet aldehydit ja ketonit liukenevat veteen, mutta ketjun pituuden kasvaessa liukoisuus vähenee.
- van der Waalsin dispersiovoimat voimistuvat molekyylien pitkittyessä.,
H-liimaus karbonyyli ryhmätasolla
Koska muodostumista H-liimaus välillä karbonyyli happi-ja vety vettä molekyyli, alempi karbonyyli-yhdisteet ovat vesiliukoisia. Mutta kun ketju kasvaa, se tulee matkalla muodostamaan vetysidoksen ja liukoisuus vähenee.
Van der Waalsin dipoli-dipoli vetovoima
Koska navat karbonyyliryhmä ja läsnäolo hajonta voimia, siellä on vetovoima välillä kaksi lähistöllä molekyylejä. Tämä saa karbonyyliyhdisteiden kiehumispisteen nousemaan korkeammalle kuin vastaavat alkaanit., Seuraavassa taulukossa huomaa, että kiehumispiste karbonyyli-yhdisteet ovat korkeammat kuin vastaavat alkaanit ja pienempi kuin alkoholit.,v>Boiling point (o C)
Spectroscopy
Infrared spectroscopy
The absorption of carbonyl group depends on the geometry of the molecule., Yleensä imeytymistä infrapuna valo osoittaa, at wavenumbers noin 1600-1900 cm−1 (5263 nm 6250 nm).
ydinmagneettinen Resonanssi
hiili-NMR-ja karbonyyli carbon osoittaa, huippu noin välillä 160-220 ppm.
