Peroksider er en gruppe av forbindelser med strukturen R−O−O−R. O−O-gruppe i en peroxide er kalt peroxide gruppe eller peroxo gruppe. I motsetning til nox-ioner, oksygen atomer i peroxide ion har en oksidasjon antall -1.,
-
InChI=1S/O2/c1-2/q-2Key: ANAIPYUSIMHBEL-UHFFFAOYSA-N
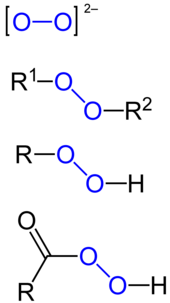
Types of peroxides, from top to bottom: peroxide ion, organic peroxide, organic hydroperoxide, peracid. The peroxide group is marked in blue. R, R1 and R2 mark hydrocarbon moieties.,
Den mest vanlige peroxide er hydrogenperoksid (H2O2), på folkemunne kjent som «skadelige». Det er markedsført som en løsning i vann ved ulike konsentrasjoner. Siden hydrogen peroxide er nesten fargeløs, så er disse løsningene. Det er i hovedsak brukt som et oksiderende og bleking agent. Imidlertid, hydrogen peroxide er også biokjemisk produsert i menneskekroppen, i stor grad som et resultat av en rekke oksidase enzymer. Konsentrerte løsninger er potensielt farlig når du er i kontakt med organiske forbindelser.,

Bortsett fra hydrogen peroxide, noen andre store klasser av peroksider er:
- Peroxy syrer, den peroxy derivater av mange kjente syrer, eksempler blir peroxymonosulfuric syre og cidex syre, og deres salter, ett eksempel er kalium peroxydisulfate.
- Hoved-gruppe peroksider, forbindelser med sammenhengen E−O−O−E (E = main gruppe-element).,
- Metal peroxides, examples being barium peroxide (BaO2), sodium peroxide (Na2O2) and zinc peroxide (ZnO2).
- Organic peroxides, compounds with the linkage C−O−O−C or C−O−O−H. One example is tert-butylhydroperoxide.
