zoals u in Figuur 1 kunt zien, variëren de nucleotiden slechts licht, en alleen in de stikstofhoudende base. In het geval van DNA, zijn die basissen adenine, guanine, cytosine, en thymine. Let op de gelijkenis van de vormen van adenine en guanine, en ook de gelijkenis tussen cytosine en thymine. A en G worden geclassificeerd als purines, terwijl C en T worden geclassificeerd als pyrimidines. Zolang we dingen benoemen, let op “deoxyribose” en “ribose”. Zoals de naam al aangeeft, is deoxyribose gewoon een ribose zonder zuurstof., Meer specifiek, waar er een hydroxylgroep verbonden aan de 2-koolstof van ribose is, is er slechts een waterstof verbonden aan de 2-koolstof van deoxyribose. Dat is het enige verschil tussen de twee suikers.
bij het willekeurig construeren van een enkele streng nucleïnezuur in vitro zijn er geen specifieke regels met betrekking tot de volgorde van de nucleotiden ten opzichte van hun basen. De identiteiten van hun stikstofhoudende basen zijn irrelevant omdat de nucleotiden door fosfodiësterbanden door de fosfaatgroep en pentose in bijlage zijn., Het wordt daarom vaak aangeduid als de suiker-fosfaat backbone. Als we het woord “fosfodiëster” opsplitsen, zien we dat het heel handig de verbinding beschrijft: de suikers zijn verbonden door twee esterbindingen ( —O—) met daartussen een fosfor. Een van de ideeën die studenten vaak verwarren is de richting van deze binding, en dus van nucleïnezuren in het algemeen. Als we het bijvoorbeeld hebben over DNA-polymerase, het enzym dat de toevoeging van nucleotiden in levende cellen katalyseert, zeggen we dat het in een 5-prime (5′) tot 3-prime (3′) richting werkt., Dit lijkt misschien geheimzinnig moleculair-bioloog-spreken, maar het is eigenlijk heel eenvoudig. Kijk nog eens naar twee nucleotiden die door de fosfodiësterbinding met elkaar zijn verbonden (figuur \(\Paginindex{1}\), linksonder). Een adeninenucleotide wordt verbonden met een cytosinenucleotide. De fosfodiësterbinding zal altijd de 5-koolstof van één deoxyribose (of ribose in RNA) verbinden met de 3-koolstof van de volgende suiker. Dit betekent ook dat aan de ene kant van een keten van gekoppelde nucleotiden, er een vrije 5′ fosfaat (-PO4) groep zal zijn, en aan de andere kant een vrije 3′ hydroxyl (-OH)., Deze bepalen de richting van een bundel van DNA of RNA.

DNA wordt gewoonlijk gevonden Als een dubbelstrengs molecuul in de cel, terwijl RNA meestal enkelstrengs is., Het is belangrijk om te begrijpen nochtans, dat onder de aangewezen voorwaarden, DNA zou kunnen worden gemaakt single-stranded, en RNA kan double-stranded zijn. In feite, zijn de molecules zo gelijkaardig dat het zelfs mogelijk is om dubbelstrengs hybride molecules met één streng van DNA en één van RNA te creëren. Interessant is dat RNA-RNA dubbele helices en RNA-DNA dubbele helices eigenlijk iets stabieler zijn dan de meer conventionele DNA-DNA dubbele helix.,
de basis van het dubbelstrengs karakter van DNA, en in feite de basis van nucleïnezuren als medium voor opslag en overdracht van genetische informatie, is base-pairing. Het Base-in paren rangschikken verwijst naar de vorming van waterstofbanden tussen adenines en thymines, en tussen guanines en cytosines. Deze paren zijn beduidend stabieler dan om het even welke vereniging gevormd met de andere mogelijke basissen. Voorts wanneer deze basepaarassociaties zich in de context van twee bundels van nucleic zuren vormen, is hun Uit elkaar plaatsen ook uniform en hoogst stabiel., Je herinnert je misschien dat waterstofbindingen relatief zwakke bindingen zijn. In de context van DNA is de waterstofbinding echter wat DNA extreem stabiel maakt en daarom zeer geschikt als opslagmedium voor genetische informatie op lange termijn. Aangezien zelfs in eenvoudige prokaryotes, dubbele helices van DNA minstens duizenden nucleotiden lang zijn, betekent dit dat er verscheidene duizenden waterstofbanden zijn die de twee bundels samen houden., Hoewel om het even welke individuele nucleotide-aan-nucleotide waterstof het binden interactie gemakkelijk tijdelijk door een lichte verhoging van temperatuur, of een minuscule verandering in de Ionische sterkte van de oplossing kan worden verstoord, vereist een volledige dubbel-helix van DNA zeer hoge temperaturen (over het algemeen meer dan 90oC) om de dubbele helix in individuele bundels volledig te denatureren.
omdat er een exacte één-op-één – koppeling van nucleotiden is, blijkt dat de twee strengen in wezen back-up kopieën van elkaar zijn-een vangnet in het geval dat nucleotiden uit één streng verloren gaan., In feite, zelfs als Delen van beide strengen beschadigd zijn, zolang de andere streng intact is in het gebied van de schade, dan is de essentiële informatie er nog steeds in de complementaire volgorde van de andere streng en kan op zijn plaats worden geschreven. Houd echter in gedachten dat terwijl één bundel van DNA aldus als “steun” van de andere kan handelen, de twee bundels niet identiek zijn – zij zijn complementair. Een interessant gevolg van dit systeem van complementaire en antiparallel strengen is dat de twee strengen elk unieke informatie kunnen dragen.,
bidirectionele genparen zijn twee genen op tegengestelde DNA-strengen, maar delen een promotor, die ertussen ligt. Aangezien DNA slechts in één richting kan worden gemaakt, 5′ aan 3′, stuurt deze bidirectionele promotor, vaak een CpG-eiland (zie volgend hoofdstuk), dus de RNA-polymerase voor elk gen in tegengestelde fysieke richtingen. Dit is getoond voor een aantal genen betrokken bij kanker (Borst, ovariaal), en is een mechanisme voor het coördineren van de uitdrukking van netwerken van genproducten.
De strengen van een dubbele DNA-helix zijn antiparallel., Dit betekent dat als we naar een dubbel-helix van DNA van links naar rechts zouden kijken, één bundel in de 5′ aan 3′ richting zou worden geconstrueerd, terwijl de complementaire bundel in de 3′ aan 5′ richting wordt geconstrueerd. Dit is belangrijk voor de functie van enzymen die DNA creëren en herstellen, zoals we binnenkort zullen bespreken. In Figuur \(\Paginindex{1}\) is de linker streng 5′ tot 3′ van boven naar beneden, en de andere is 5′ tot 3′ van onder naar boven.
vanuit een fysiek standpunt zijn DNA-moleculen negatief geladen (al die fosfaten), en normaal gesproken een dubbele helix met een rechtshandige twist., In deze normale (ook genoemd de “B” Bouw) staat, omvat één volledige draai van de molecule 11 basisparen, met 0.34 nm tussen elke nucleotidebasis. Elk van de stikstofhoudende basissen is vlak, en wanneer in paren gerangschikt met de aanvullende basis, vormt een bij vlakke “sport” op de “ladder” van DNA. Deze zijn loodrecht op de longitudinale as van DNA. Het grootste deel van vrij-drijvend DNA in een cel, en het meeste DNA in om het even welke waterige oplossing van dichtbij-fysiologische osmolariteit en pH, wordt gevonden in deze Bouw b., Er zijn echter andere conformaties gevonden, meestal onder zeer specifieke omgevingsomstandigheden. Een gecomprimeerde Bouw, a-DNA, werd waargenomen als een Artefact van in vitro kristallisatie, met iets meer basissen per beurt, kortere Draailengte, en basenparen die niet loodrecht op de longitudinale as zijn. Een ander, Z-DNA, lijkt zich tijdelijk te vormen in GC-rijke stukken DNA waarin, interessant genoeg, het DNA de tegenovergestelde richting verdraait.
Er is gesuggereerd dat zowel de A-als de Z-vorm van DNA in feite fysiologisch relevant zijn., Er is bewijsmateriaal om voor te stellen dat de A vorm in de hybride dubbele helices van RNA-DNA evenals kan voorkomen wanneer DNA aan sommige enzymen wordt gecomplexeerd. De Z-bouw kan in reactie op methylation van DNA voorkomen. Bovendien is de “normale” B-DNA-Bouw iets van een geïdealiseerde structuur gebaseerd op volledig gehydrateerd zijn, zoals zeker zeer waarschijnlijk binnen een cel is. Die hydratatietoestand verandert echter voortdurend, zij het minutieus, dus de DNA-conformatie zal vaak licht afwijken van de B-conformatie parameters in Figuur \(\Paginindex{2}\).,
bij prokaryoten wordt het DNA gevonden in het cytoplasma (vrij duidelijk omdat er geen andere keuze is in deze eenvoudige organismen), terwijl bij eukaryoten het DNA in de kern wordt gevonden. Ondanks de verschillen in hun plaatsen, wordt het niveau van bescherming tegen externe krachten, en vooral, hun grootte, zowel prokaryotic als eukaryotic DNA verpakt met proteã nen die helpen om de Algemene chromosoomstructuur te organiseren en te stabiliseren., Relatief weinig wordt begrepen met betrekking tot prokaryotic chromosomale verpakking hoewel er structurele gelijkenissen tussen sommige proteã nen in prokaryotic en eukaryotic chromosomen worden gevonden. Daarom, de meeste inleidende celbiologie cursussen vasthouden aan eukaryotic chromosomale verpakking.

naakt DNA, hetzij prokaryotisch of eukaryotisch, is een extreem dunne streng materiaal met een diameter van ongeveer 11 nm. Nochtans, gegeven de grootte van eukaryotic genomen, als DNA op die manier binnen de kern werd opgeslagen, zou het onbeheersbaar verward worden. Beeld een emmer waarin u hebt gegooid een honderd meter van garen zonder enige poging om het te organiseren door het oprollen of bunching het., Overweeg nu of je in staat zou zijn om te bereiken in die emmer trek op een streng, en verwachten te trekken slechts één streng, of als in plaats daarvan bent u waarschijnlijk te trekken ten minste een kleine wirwar van garen. De cel doet in wezen wat je zou doen met het garen om het georganiseerd te houden: het is netjes verpakt in kleinere, beheersbare strengen. In het geval van DNA, wordt elk chromosoom van een lus voorzien rond een histone complex om de eerste orde van chromosomale organisatie te vormen: het nucleosoom.
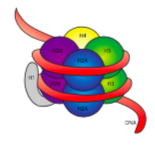
de Vezel van 30 nm wordt bij elkaar gehouden door twee sets interacties. Eerst brengt linker histone, H1, de nucleosomen samen in een ongeveer 30 nm structuur., Deze structuur wordt dan gestabiliseerd door disulfidebanden die tussen H2A histone van één nucleosoom en H4 histone van zijn buurman vormen.
histonen zijn een familie van basische (positief geladen) eiwitten. Zij allen functioneren hoofdzakelijk in het organiseren van DNA, en het nucleosoom wordt gevormd wanneer DNA (iets meer dan 2 keer) rond een kern van acht histones – twee elk van H2A, H2B, H3, en H4 wikkelt. Het aantal en de positie van de positieve ladingen (meestal van lysines en arginines) zijn cruciaal voor hun capaciteit om DNA strak te binden, dat zoals eerder vermeld, zeer negatief geladen is., Dat “tegenpolen aan te trekken” idee is niet alleen een dating tip uit de adviezen columns.

na onderzoek van de 3D-structuur van het histonkerncomplex, zien we dat terwijl relatief ongeladen eiwitinteractiedomeinen de histonen in het centrum bij elkaar houden, de positief geladen residuen rond de buitenkant van het complex worden gevonden, die beschikbaar zijn om te interageren met de negatief geladen fosfaten van DNA.,
in een later hoofdstuk zullen we bespreken hoe enzymen het DNA lezen om de informatie te transcriberen op kleinere, meer beheersbare stukken RNA. Voor nu hoeven we ons er alleen maar van bewust te zijn dat op een gegeven moment veel van het DNA stevig is verpakt, terwijl sommige delen van het DNA dat niet zijn. Omdat de onderdelen die beschikbaar zijn voor gebruik kunnen variëren afhankelijk van wat er gebeurt met/in de cel op een bepaald moment, moet de verpakking van DNA dynamisch zijn. Er moet een mechanisme zijn om de band van DNA aan histones snel los te maken wanneer dat DNA voor genuitdrukking nodig is, en om de band aan te halen wanneer het niet is., Aangezien het blijkt, impliceert dit proces acetylation en deacetylation van de histones.

Histone Acetyltransferases (HATs) zijn enzymen die een acetylgroep op een lysine van een Histon-eiwit plaatsen. De acetylgroepen zijn negatief geladen, en acetylation voegt niet alleen een negatief geladen groep toe, verwijdert het ook de positieve last van lysine. Dit heeft niet alleen het effect van het neutraliseren van een punt van aantrekking tussen het eiwit en het DNA, maar zelfs enigszins afstoten (met soortgelijke ladingen)., Aan de andere kant van het mechanisme, Histone Deactylases (HDACs) zijn enzymen die de acetylering verwijderen, en daardoor de interactie tussen histone proteã ne en DNA herstellen. Aangezien dit zulke belangrijke enzymen zijn, staat het aan reden dat zij niet worden toegestaan om willens en wetens op om het even welke beschikbare histone te werken, en in feite, worden zij vaak gevonden in complex met andere proteã nen die hun activering met andere processen zoals activering van transcriptie controleren en coördineren.
