Nach Richtlinien der American Thoracic Society (ATS) und der Infectious Disease Society of America (IDSA) sollten posteroanterior (PA) Thorax-Röntgenaufnahmen erhalten werden, wenn bei Erwachsenen eine Lungenentzündung vermutet wird. Nach Möglichkeit sollten auch seitliche Bilder aufgenommen werden.
Die radiologischen Befunde der adulten Viruspneumonie sind variabel und überlappend. Die Korrelation zwischen pathologischen und radiologischen Befunden ist gut., Da es sich bei den Viren um intrazelluläre Erreger handelt, treten die meisten pathologischen Veränderungen im Umfeld der Viruspneumonie im Epithel und im angrenzenden interstitiellen Gewebe auf. Je nach Virulenz und Infektionsrate können 2 Arten von pathologischen Reaktionen und radiologischen Aspekten beobachtet werden: (1) üblicher, langjähriger oder heimtückischer Verlauf einer Lungenentzündung; und (2) schnell fortschreitende oder virulente Lungenentzündung.
Die übliche Form (langjähriger oder heimtückischer Verlauf der Lungenentzündung) ist durch lymphatische Infiltrate in den Alveolarsepten gekennzeichnet., Diese erstrecken sich manchmal auf die Lunge neben den terminalen und respiratorischen Bronchiolen oder in seltenen Fällen sogar auf den gesamten Läppchen. In radiologischen Studien erscheinen diese Befunde als 4-bis 10-mm -, schlecht definierte Knötchen und fleckige Bereiche der peribronchialen Boden-Glas-Opazität und Luftraumkonsolidierung mit variabler Hyperinflation.,
Die schnell fortschreitende oder virulente Pneumonie mit diffuser Alveolarblutung erstreckt sich auf das Interstitium und den Luftraum (mit interstitiellem Infiltrat, Luftraumblutung, Ödem, Fibrin, Typ-2-Pneumozytenhyperplasie, hyaliner Membranbildung). Das Röntgenbild der Brust zeigt den schnellen Zusammenfluss von lückenhaften, einseitigen oder bilateralen Konsolidierungen und Bodenglasopazität oder schlecht definierten zentrilobulären Knötchen.,
Adenovirus-Pneumonie
Pathologische Befunde einer adenoviralen Pneumonie werden durch fleckige Bereiche hämorrhagischer Konsolidierung dargestellt, die sich zu Nekrose und diffuser Alveolarblutung, nekrotisierender Bronchiolitis mit Überinflation und Atelektase entwickeln. Die üblichen radiologischen Befunde sind diffuse bilaterale Bronchopneumonie und schwere Überinflation. Lobarkollaps und Atelektase ist eine häufige Komplikation; Die Atelektase des rechten Oberlappens ist am häufigsten bei Säuglingen und der Kollaps des linken Unterlappens ist bei älteren Kindern häufig., Radiologische Veränderungen lösen sich in unkomplizierten Fällen in 2 Wochen auf.
Etwa 53% der Kinder mit akuter adenoviraler Pneumonie entwickeln eine Form chronischer Erkrankung: Bronchiektasen, obliterative Bronchiolitis, interstitielle Fibrose oder einseitiges hyperluzentes Lungensyndrom. Ungefähr 64% der komplizierten Fälle werden bei Kindern unter 2 Jahren beschrieben.
Bei Lungentransplantationsempfängern ist die adenovirale Pneumonie am schwersten mit der höchsten Sterblichkeitsrate im Vergleich zu Patienten mit anderen Atemwegsviren., Es wurde festgestellt, dass die radiologischen Befunde typischerweise schwerwiegender sind als bei RSV-oder PIV-Pneumonie. Änderungen bestehen aus fortschreitenden homogenen Konsolidierungen, die sich über Tage oder Wochen entwickeln. Pleuraergüsse werden bei 20% der Patienten beobachtet.
CMV-Pneumonie
Die pathologischen Befunde bei CMV-Pneumonie unterscheiden sich je nach Grad der Immunsuppression des Wirts., Bei mäßig immungeschwächten Transplantationspatienten sind die interstitielle Pneumonie, entzündliche oder hämorrhagische Knötchen, organisierte Pneumonie und schwere nekrotisierende Pneumonie auf einen T-Zell–vermittelten Immunmechanismus zurückzuführen.
Patienten mit erhöhter Immunsuppression, wie solche mit AIDS, haben eine hohe Dichte an CMV-Einschlusskörpern. Diese sind direkt verantwortlich für schwere Pneumonitis oder diffuse Alveolarschäden. Bei Empfängern von Festorgantransplantationen erscheint CMV-Pneumonie häufig normal oder minimal abnormal auf Röntgenaufnahmen der Brust., Bei einer Reihe von Lungentransplantationsempfängern mit nachgewiesener CMV-Pneumonitis hatte nur ein Drittel der Patienten abnormale Röntgenaufnahmen. In der Gruppe mit normalen Röntgenaufnahmen wurden keine Todesfälle registriert, verglichen mit der 18% igen Mortalität in der Gruppe mit Röntgenanomalien.
Wenn abnormal, brust röntgenaufnahmen zeigen eine interstitielle muster der krankheit, die ist in der regel diffus und die beinhaltet die basen. Das interstitielle Muster besteht aus der Akzentuierung der Kerley A-und Kerley B-Linien oder aus diffusen, dunstigen, gemahlenen Glastrübungen.,
Relativ wenige Berichte weisen auf eine CMV-Pneumonie bei immunkompetenten Wirten hin. Interstitielle Infiltrate wurden bei einigen Patienten aus einer Reihe von 34 immunkompetenten Patienten beschrieben.
Coxsackievirus-Pneumonie
In den wenigen gemeldeten Fällen einer Coxsackievirus-Pneumonie besteht das Röntgenbild aus einer feinen perihilaren Infiltration. In den Fällen mit Pleurodynie kann eine Parenchymkonsolidierung in den Lungenbasen beobachtet werden.,
EBV-Pneumonie
Die Beteiligung der EBV-Lunge ist durch mononukleäre Infiltrate in bronchovaskulären Bündeln und interlobulären Septen sowie in Alveolarexsudaten gekennzeichnet. Die Röntgenanalyse der Brust in 59 Fällen von infektiöser Mononukleose ergab eine Splenomegalie als häufigsten Befund (47%), gefolgt von einer Vergrößerung des hilaren Lymphknotens (13%), einem diffusen retikulären Muster, das auf eine interstitielle Erkrankung hinweist (5%) und bilaterale oder einseitige Pleuraergüsse.,
Lungenkonsolidierung bei infektiöser Mononukleose im Zusammenhang mit interstitiellen Lungeninfiltraten ist selten.
Echovirus-Pneumonie
Echovirus-Pneumonie weist ein Muster erhöhter bronchovaskulärer Markierungen und bilateraler hilarer Lymphknotenvergrößerung auf.
Rhinovirus-Pneumonie
Alveoläre und / oder interstitielle Lungeninfiltrate, Konsolidierung und komplizierte Bronchiolitis sind die häufigsten Befunde für Rhinovirus-Pneumonie. Pleuraergüsse sind seltener.,
Hantavirus-Pneumonie
Wie bei anderen viralen Ätiologien treten bei der Hantavirus-Pneumonie interstitielle und Luftraumödeme, interstitielle Lymphozyteninfiltrate, Epithelnekrose und Gefäßthrombose auf. Besondere Aspekte von hantaviralen Läsionen sind ausgedehnte Zelltrümmer mit Zerstörung von Typ-I-Zellen und einer Dominanz von Typ-II-Pneumozyten, neutrophilen Infiltraten und fibrosierender Alveolitis.,
Röntgenaufnahmen des Brustkorbs zeigen interstitielle Ödeme mit oder ohne Progression zur Luftraumkrankheit mit einer zentralen oder bibasilären Verteilung und gemeinsamen Pleuraergüssen. Das Lungenkapillarlecksyndrom einer hantaviralen Infektion kann sekundär zum damit verbundenen Nierenversagen sein.,
HIV-Pneumonie
Feine retikuläre oder retikulonoduläre Infiltrate im Lungeninterstitium und grobe retikulonoduläre Infiltrate oder Trübungen mit überlagerten fleckigen Alveolarinfiltraten wurden bei Patienten mit AIDS oder AIDS-bedingtem Komplex (ARC) und Biopsie-nachgewiesener lymphozytärer interstitieller Pneumonie beschrieben. Diese Krankheit wird als gutartige Reaktion von bronchialassoziiertem Lymphgewebe auf HIV angesehen. Röntgenbefunde sind während des gesamten Krankheitsverlaufs bei 75% der Patienten stabil.,
HSV-Pneumonie
Die HSV-Pneumonie ist in der Regel durch alveoläre Nekrose und proteinartige Exsudate mit oder ohne nekrotisierende Bronchopneumonie gekennzeichnet. Es wird angenommen, dass die fokalen Infiltrate Ausdruck von aspirierten Sekreten sind, und die diffusen bilateralen Infiltrate spiegeln die hämatogene Ausbreitung wider.
Eine Studie an 23 Patienten mit HSV-1-Pneumonie zeigte lückenhafte segmentale oder subsegmentale Luftraumtrübungen in 100% und eine Lobarverteilung und Bodenglastrübungen in 48%. Etwa 30% der Patienten hatten zusätzliche retikuläre Trübungen., Das Muster war diffus und multifokal in allen, verstreut in 82%, peripher in 9% und zentral in 4%. Pleuraergüsse wurden in 52% nachgewiesen. Der Nachteil dieser Studie war, dass einige der bilateralen Konsolidierungen möglicherweise sekundär zu ARDS und nicht zu einer HSV-Infektion waren.
Eine weitere Studie an 17 Patienten mit HSV-Pneumonie ergab keine hohe Korrelation zwischen ARDS und HSV-Pneumonie. Die meisten konsistente Ergebnisse wurden bilaterale Trübung mit einer air-space (3 von 14) oder einer gemischten Luftraum und interstitial-Muster (8 von 14)., Das Muster der Trübungen war bilateral und diffus (12 von 14), und das Ausmaß war lobar (6 von 14), oder es umfasste fast die gesamte Lunge (6 von 14). Pleuraergüsse (meist moderat) wurden bei 8 Patienten beschrieben, und Atelektasen wurden bei 5 gefunden. Das Vorhandensein von 2 normalen Brustaufnahmen in dieser Serie kann durch die Kontamination von BAL-Proben aus den oberen Atemwegen erklärt werden.,
Bei Neugeborenen mit HSV-2-Infektion, die während der Entbindung kontrahiert wurden, wird eine fortschreitende Entwicklung von einem normalen Thorax-Röntgenbild zu interstitiellen Veränderungen, Luftraumkonsolidierung und diffuser Konsolidierung beider Lungen beschrieben. Die interstitielle Erkrankung ist diffus, meist bilateral, mit Granularität und linearen und undurchsichtigen Strängen in hilaren und peribronchialen Bereichen. Diffuse Alveolarinfiltrate erhöhen die Trübung der Lunge ohne Volumenverlust. Diffuse Konsolidierung ist der Ausdruck von Lungenblutungen mit nekrotisierender Pneumonitis. Pleuraergüsse können gesehen werden.,
Bei einer Reihe von 42 Patienten mit HSV-Pneumonie zeigten alle Röntgenaufnahmen Anomalien: Lungeninfiltrate (93%), Pleuraergüsse (29%) und Atelektasen (12%). Bei einer Reihe von 7 Patienten mit HSV-Pneumonie nach Herztransplantation hatten 5 diffuse bilaterale Veränderungen, entweder gemischt interstitiell mit einem Luftraum oder interstitiell und mikronodular.,
Influenza-Virus – Pneumonie
Röntgenologische Veränderungen der Brust bei Influenza-Pneumonie (im Bild unten zu sehen) reichen von leichter interstitieller Prominenz über schlecht definierte, 1 bis 2 cm lückenhafte Konsolidierungsbereiche bis hin zu ausgedehnten Luftraumerkrankungen aufgrund eines hämorrhagischen Lungenödems. Alveolarblutung kann als kleine zentrilobuläre Knötchen gesehen werden. Pleuraerguss ist selten und stellt normalerweise eine bakterielle Infektion dar. Hohlraumbildung deutet auf bakterielle Superinfektion mit Staphylokokken-Organismen hin.,
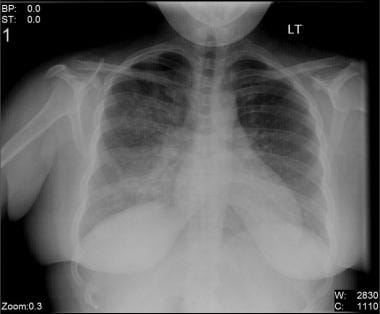 Bilaterale interstitielle Infiltrate in einem 31-jährigen Patienten mit influenza-Pneumonie.
Bilaterale interstitielle Infiltrate in einem 31-jährigen Patienten mit influenza-Pneumonie. Die radiologischen Befunde bei Lungentransplantationsempfängern mit Influenza-Pneumonie sind unspezifisch und reichen von subtilen heterogenen und linearen Trübungen bis hin zu homogenen Lobarkonsolidierungen, an denen die unteren Lappen stärker beteiligt sind als die oberen Lappen. Röntgenaufnahmen der Brust Infiltrate werden bei 36% der infizierten Patienten gesehen. Patienten mit röntgenologischen Veränderungen der Brust scheinen schwerwiegendere Ergebnisse zu haben als die anderer Patienten.,
In einer retrospektiven Einzeluntersuchung waren Luftraumkonsolidierungen (89%) und peribronchiale Bodenglastrübungen (89%), die vorwiegend mittlere und untere Lungenzonen betrafen, die häufigsten bildgebenden Befunde bei Patienten mit H1N1-Pneumonie, die auf die Intensivstation eingeliefert wurden. Ergebnisse wurden zweiseitig in 94% der Patienten.
Masern-Virus-Pneumonie
Primäre Masern-Pneumonie führt zu gemischten Netzhauttrübungen und Luftraumkonsolidierung. Lymphknotenvergrößerung im Hilum kann bei Kindern gesehen werden., Die pathologische Grundlage für diese Befunde ist die epitheliale Hyperplasie in Bronchiolen und peribronchialen Alveolen, mehrkernigen Riesenzellen in den Alveolen und diffusen Alveolarschäden.
Atypische Masernpneumonie tritt mit sphärischer oder segmentaler Konsolidierung auf, die sich schnell klärt. Hilar Lymphknotenvergrößerung und Pleuraerguss sind häufig assoziiert.
Lungenentzündung aufgrund bakterieller Superinfektion ist segmental verteilt, betrifft 1 oder beide untere Lappen und ist häufig mit Atelektasen verbunden., Das Vorhandensein einer dichten Opazität deutet eher auf eine bakterielle Ätiologie hin (88%) als auf eine virale Ätiologie (36%).
PIV-Pneumonie
Radiographische Veränderungen der PIV-Pneumonie sind relativ unspezifisch und bestehen aus diffuser oder fokaler Akzentuierung von Lungenmarkierungen, die durch peribronchiale oder peribronchioläre Infiltration in den unteren Lappen verursacht werden.
Die durch PIV-3 hervorgerufene Riesenzellpneumonie kann durch Alveolarproteinose kompliziert sein; 1 Fall wird bei einem Empfänger von transplantiertem Nabelschnurblut berichtet., Der radiologische Aspekt war unspezifisch und bestand aus bilateralen lückenhaften Infiltraten.
RSV-Pneumonie
Das radiologische Muster der RSV-Pneumonie ist Ausdruck von Schleimhautnekrose und interstitieller Entzündung, die mit Bronchialverengung und Okklusion und Bronchialwandverdickung einhergehen. Das typische radiologische Erscheinungsbild einer RSV-Infektion der unteren Atemwege ist noch nicht genau definiert. Die typischen Befunde gelten nach wie vor als unspezifisch.,
Eine Studie aus dem Jahr 1974 an 126 Kindern mit akuter RSV-Infektion der unteren Atemwege zeigte typische Merkmale eines Kollapses oder Airtrapping in kleinen Konsolidierungsbereichen. Airtrapping und Peribronchitis war am häufigsten bei Säuglingen jünger als 6 Monate, während Konsolidierung wurde am häufigsten nach dem Alter von 6 Monaten gesehen. Atelektase war ein seltener Befund und korrelierte nicht mit dem Alter.
Andere Autoren zeigten, dass die Variabilität der Lungeninfiltration mit der Schwere der Infektion korreliert., Atelektase ist häufiger bei Kindern mit positiven Bakterienabstrichen als bei anderen. (Die Lungeninfiltration wird im Bild unten gezeigt.)
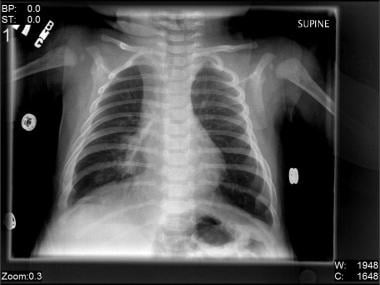 Infiltrat des rechten Mittellappens bei einem 2 Monate alten Jungen mit Lungenentzündung durch Respiratory Syncytial virus (RSV).
Infiltrat des rechten Mittellappens bei einem 2 Monate alten Jungen mit Lungenentzündung durch Respiratory Syncytial virus (RSV). Lobaremphysem kann mit RSV-Pneumonie assoziiert sein.
Eine Studie mit 128 Röntgenaufnahmen der Brust von Kindern mit einer Infektion der unteren Atemwege zeigte hauptsächlich lobare Pneumonie, Bronchopneumonie oder normale Befunde bei Säuglingen unter 6 Monaten., Kinder älter als diese hatten hauptsächlich Peribronchitis oder interstitielle Pneumonie, wie auf den Brustbildern dargestellt.
Eine in Deutschland durchgeführte Studie zeigte 3 wichtige radiologische Befunde in 108 Fällen einer bestätigten RSV-Infektion der unteren Atemwege: normale Röntgenergebnisse der Brust (30%), zentrale Pneumonie (32%) und Peribronchitis (26%). Weitere Befunde waren Emphysem (11%), Pleuraerguss (6%), Bronchopneumonie (6%), Atelektase (5%) und Pneumothorax (0,9%). Altersspezifische Unterschiede wurden nicht bestätigt., Empfindliche Labortests zur Bestätigung einer RSV-Infektion und zum Ausschluss einer bakteriellen Superinfektion können die Unterschiede zwischen dieser und früheren Studien erklären.
Bei Erwachsenen wird der Röntgenaspekt häufig durch bakterielle Infektionen erschwert. In einer Studie in Ohio hatten 40% Patienten Anzeichen einer Lungenentzündung oder Konsolidierung; In 35% wurde eine Lobarverteilung beobachtet. Pleuraergüsse werden in 5% der Fälle gesehen.
Bei Lungentransplantationsempfängern sind RSV-und PIV-Pneumonien tendenziell weniger symptomatisch und ohne radiologische Befunde., Autoren haben diffuse homogene Konsolidierungen bei ähnlichen Patienten beschrieben.
SARS-Virus Pneumonie
Seit Ausbruch der ersten Ausbrüche in Asien und später in Kanada im Jahr 2003 wurden umfangreiche Berichte über radiologische Befunde bei SARS veröffentlicht. Pathologische Veränderungen von SARS bestehen aus diffusen Alveolarschäden mit einer kleinen Menge interstitiellem lymphozytischem Infiltrat. Die frühe Phase ist durch Lungenödem mit hyaliner Membranbildung gekennzeichnet, und die Organisationsphase ist durch zelluläre fibromyxoid organisierende Luftraumexsudate gekennzeichnet., Diese Ergebnisse erklären, warum die meisten Bilder von Patienten, die mit einer SARS-Infektion aufgenommen wurden, unspezifisch und nicht von denen anderer viraler oder bakterieller Bronchopneumonien zu unterscheiden sind.
Bei Patienten mit negativen radiologischen Befunden kann die Erkrankung nicht ausgeschlossen werden. Röntgenuntersuchung, dynamische Beobachtung und digitale Radiographie können verwendet werden, um die Testempfindlichkeit zu erhöhen. Die meisten Autoren betonen die Notwendigkeit serieller Röntgenaufnahmen der Brust.
Eine Studie an 13 kanadischen Gesundheitspersonal mit wahrscheinlichen SARS ergab 3 unverwechselbare radiographische Muster., Das häufigste Muster (gesehen in 76,9% der Fälle) war die fokale periphere Luftraumkrankheit bei Präsentation mit allmählicher Auflösung. Einige Patienten hatten anfangs normale Röntgenaufnahmen: 15, 4% entwickelten später eine fokale Luftraumkrankheit und 7, 7% hatten eine runde Lungenentzündung, ein seltener Befund, der durch andere Studien bestätigt wurde. Bilaterale Erkrankungen wurden bei 53,8% der Patienten beobachtet, und eine einseitige Beteiligung wurde bei 46,2% beobachtet. Alle Patienten hatten eine Luftraumkrankheit der mittleren und unteren Lunge und 46, 2% hatten zusätzliche Infiltrate der oberen Lunge., Es wurden keine Hinweise auf Pleuraverdickung, Erguss, Lymphadenopathie, Hohlräume oder klinisch signifikante Atemwegsveränderungen gefunden.
Eine retrospektive Studie an 62 Kindern mit SARS aus Kanada, Singapur und Hongkong ergab bei 35, 5% normale Röntgenaufnahmen der Brust. Prominente radiologische Befunde bei den übrigen Kindern waren Bereiche der Konsolidierung (Boden-Glas-Trübungen oder fokale, lobare oder multifokale Trübungen; 45,2%), die oft peripher und in den unteren Lappen waren. Peribronchiale Verdickung wurde in 14,5% festgestellt. Radiologische Beweise für Adenopathie wurden nicht gesehen., Laut den Autoren hat die Radiographie zwei Hauptrollen in SARS. Die erste besteht darin, die pulmonale Beteiligung in den Verdachtsfällen von SARS darzustellen, und die zweite besteht darin, radiologische Veränderungen zu zeigen, die für andere bakterielle oder granulomatöse Erkrankungen charakteristisch sind. Ausgedehnte Pleuraergüsse, Pneumothorax, Pneumatozele, Lungenabszess, Kavitation und Adenopathie sind seltene radiologische Befunde bei SARS.,
VZV-Pneumonie
VZV-Invasion der Lunge verursacht Schwellungen, Proliferation von Typ-II-Zellen, Endothelschäden in den kleinen Blutgefäßen und Desquamation von Alveolarseptumzellen mit Alveolarseptummononukleärer Infiltration. Fibrinöses Exsudat, das in hyalinen Membranen vorkommt, und fokale hämorrhagische Nekrose sind häufig.
Nachdem sich der Patient von der ursprünglichen Krankheit erholt hat, sind sphärische Knötchen zu sehen. Sie bestehen aus einer äußeren, faserigen, Lamellatkapsel, die Bereiche von hyalinisiertem Kollagen oder nekrotischem Gewebe mit variablem Verkalkungsgrad umschließt.,
Das Röntgenbild ist verstreut, schlecht definiert, 5-bis 15-mm-Knotentrübungen (azinares Knotentrübenmuster). Diese sind konfluent und flüchtig und identisch in immunkompetenten und immungeschwächten Wirten. Die Knötchen sind in der Lungenperipherie (Basen) zu sehen, die in der Nähe der Hila koaleszieren; Diese spiegeln wahrscheinlich die zusammenhängende Ausbreitung der Tracheobronchitis wider. Retikuläre Markierungen, Pleuraergüsse und hilare Adenopathie werden selten gesehen.
Die radiologischen Manifestationen treten normalerweise 2-5 Tage nach dem Hautausschlag auf., Sie neigen dazu, in 3-5 Tagen bei leichter Krankheit zu löschen und nehmen bis zu mehreren Wochen oder Monaten in weit verbreiteten Krankheit zu löschen.
Eine scheinbar einzigartige Komplikation der akuten VZV – Pneumonie besteht aus dem späten Auftreten (Jahre nach Beginn der Lungenentzündung) von 2-bis 3-mm-dichten Verkalkungen, die in der unteren Lungenhälfte gut definiert, verstreut und vorherrschend sind. Die Häufigkeit dieser Verkalkungen beträgt 1,7-2,0% bei Erwachsenen mit vorheriger VZV-Pneumonie.,
Vertrauensgrad
Mehrere Berichte deuten darauf hin, dass die Thoraxradiographie nicht zur Unterscheidung von nichtbakterieller Pneumonie von bakterieller Pneumonie verwendet werden kann. Die begrenzte Anzahl der verwendeten Patienten und mikrobiologischen Techniken und die große Variation der deskriptiven radiologischen Begriffe beschränkten die Ergebnisse, und es können keine allgemeinen Schlussfolgerungen gezogen werden.
Das Erreichen einer Standardisierung der radiologischen Ergebnisberichterstattung ist wichtig, um Vertrauen in die Interpretation der Lungenentzündungsätiologie zu schaffen., Die BARSCH-Studie bekräftigte die Ergebnisse, dass die Beobachtervereinbarung am besten für die Konsolidierung und am schlechtesten für die Ergebnisse anderer Infiltrate geeignet ist.
Eine Gruppe aus Finnland meldete 215 Kinder mit CAP an. Ihre Ergebnisse zeigten, dass 71% der Kinder mit alveolären (insbesondere lobaren) Infiltraten, wie auf Röntgenaufnahmen der Brust gezeigt, Anzeichen einer bakteriellen Infektion aufwiesen. Eine Hälfte der Kinder mit interstitiellen Infiltraten als einziger radiologischer Befund hatte eine bakterielle Infektion. Daher waren interstitielle Infiltrate kein zuverlässiger Hinweis auf eine virale Pneumonie.,
Eine spezifische Organismus-Diagnose einer viralen Pneumonie kann nicht allein anhand von bildgebenden Merkmalen gestellt werden. Die radiologischen Manifestationen hängen vom immunologischen Status des Patienten und vorbestehenden oder koexistierenden Lungenerkrankungen ab. Viele Krankheitserreger können sich überlappende radiologische Merkmale aufweisen, und nicht alle Ärzte sind sich über die Bedeutung einiger beschreibender Begriffe einig. Die bildgebenden Aspekte sollten in klinische und epidemiologische Daten integriert und durch virologische Tests bestätigt werden., Die Erkennung der radiologischen Befunde hilft bei der Verengung der Differentialdiagnose und bei der Beurteilung der Krankheitsentwicklung und Komplikationen.
