Vorhersage von SN1-vs. SN2-Mechanismen
Wenn man bedenkt, ob eine nukleophile Substitution wahrscheinlich über einen SN1-oder SN2-Mechanismus auftritt, müssen wir wirklich drei Faktoren berücksichtigen:
1) Das Elektrophil: Wenn die Proteingruppe an eine Methylgruppe oder einen Primärkohlenstoff gebunden ist, wird ein SN2-Mechanismus bevorzugt (hier ist das Elektrophil und jeder Carbocation-Zwischenstopp wäre energiereich und daher unwahrscheinlich)., Wenn die Leaving-Gruppe an einen tertiären, Allyl-oder Benzylic-Kohlenstoff gebunden ist, wird ein Carbocation-Zwischenprodukt relativ stabil sein und somit wird ein SN1-Mechanismus begünstigt. Diese Muster der Reaktivität von unten zusammengefasst.,yl Halogenid Struktur
2) Das Nucleophile: starke Nucleophile, insbesondere solche mit negativen Ladungen, begünstigen das SN2 mechanismus., Schwächere Nukleophile wie Wasser oder Alkohole begünstigen den SN1-Mechanismus.
3) Das Lösungsmittel: Polare aprotische Lösungsmittel begünstigen den SN2-Mechanismus, indem sie die Reaktivität des Nukleophilen erhöhen. Polare protische Lösungsmittel begünstigen den SN1-Mechanismus, indem sie den Übergangszustand und das Carbokationszwischenprodukt stabilisieren. SN1-Reaktionen werden Solvolyse-Reaktionen genannt, wenn das Lösungsmittel das Nukleophile ist.
Diese Reaktivitätsmuster sind in der nachstehenden Tabelle zusammengefasst.,>
For example, the reaction below has a tertiary alkyl bromide as the electrophile, a weak nucleophile, and a polar protic solvent (we’ll assume that methanol is the solvent)., So würden wir zuversichtlich einen SN1-Reaktionsmechanismus vorhersagen. Da Substitution bei einem chiralen Kohlenstoff auftritt, können wir auch vorhersagen, dass die Reaktion mit Racemisierung fortfahren wird.

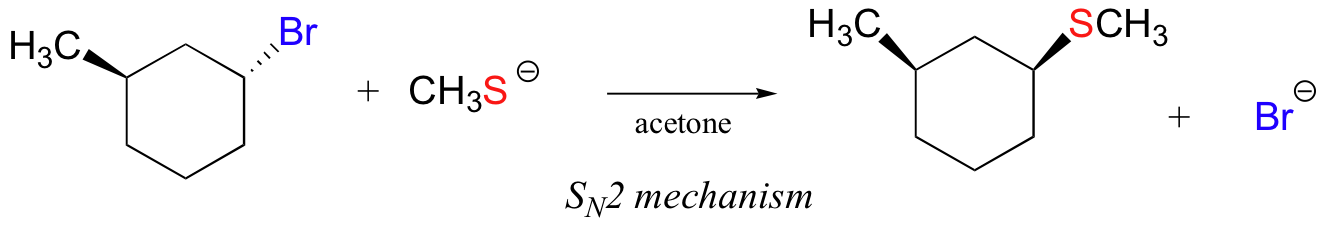
In der folgenden Reaktion ist das Elektrophil dagegen ein Sekundäralkylbromid – mit diesen sind sowohl SN1-als auch SN2-Mechanismen möglich, abhängig vom Nucleophilen und dem Lösungsmittel. In diesem Beispiel ist das nukleophile (ein Thiolatanion) stark, und ein polares protisches Lösungsmittel wird verwendet – so wird der SN2-Mechanismus stark bevorzugt., Es wird erwartet, dass die Reaktion mit einer Inversion der Konfiguration fortschreitet.
Übung
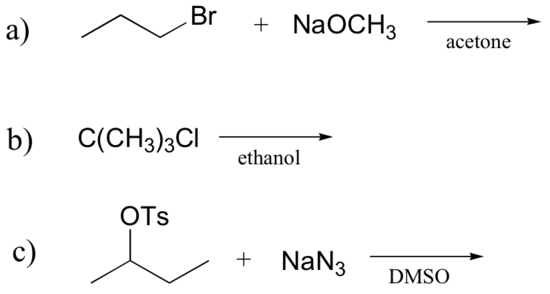
1. Bestimmen Sie, ob jede Substitutionsreaktion, die unten gezeigt wird, wahrscheinlich durch einen SN1-oder SN2-Mechanismus abläuft, und erläutern Sie Ihre Argumentation.
Antwort
a) SN2 b/c Primäralkylhalogenid mit einem starken Nucleophilen in einem polaren aprotischen Lösungsmittel.
b) SN1 b / c tertiäres Alkylhalogenid mit einem schwachen Nucleophilen, das auch das Lösungsmittel ist (Solvolyse).,
c) SN2 b / c sekundäre Alkylhalogenide begünstigen diesen Mechanismus, wenn sie mit einem starken Nukleophilen (und einer schwachen Base) in einem polaren aprotischen Lösungsmittel reagiert werden.
