eksempel – forudsigelse af Molekylær polaritet:
afgør, om molekylerne repræsenteret ved følgende formler er polære ellernonpolære. (Du skal muligvis tegne Le .is strukturer og geometriske skitser til doso.)
a. CO2 b. OF2 c. CCl4 d. CH2Cl2 e. HCN
løsning:
A. Le Theis-strukturen for CO2 er
elektronegativiteten af kulstof og ilt er 2,55 og 3,44. Den 0.,89 forskel i elektronegativitet indikerer ATEC – o-bindinger er polære, men det symmetriske arrangement af disse bindinger gørmolekylet ikke-polært.
Hvis vi sætter Pile ind i den geometriske skitse for CO2, ser vi, at de nøjagtigt balancerer hinanden, i både retning ogstorhed. Dette viser bindingernes symmetri.
b., Le .is-strukturen for OF2 er
elektronegativiteten af O .ygen og fluor,henholdsvis 3.44 og 3.98, producerer en 0.54 forskel, der får os til at forudsige, at O-f-bindingerne er polære. Den molekylære geometri af OF2 er bøjet. Suchan asymmetrisk fordeling af polære bindinger ville producere et polært molekyle.
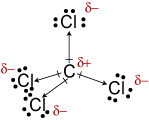
c. den molekylære geometri af CCl4 istetrahedral., Selvom C-Cl-bindingerne er polære, deres symmetriske arrangementgør molekylet ikke-polært.
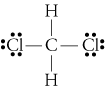
d. ch2cl2 er
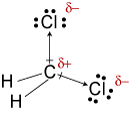
elektronegativiteten af hydrogen, carbon ogchlorin er 2,20, 2,55 og 3,16. 0,35 forskellen i elektronegativitet forhc-obligationerne fortæller os, at de i det væsentlige er ikke-polære. Den 0.,61forskellen i elektronegativitet for C-Cl-bindingerne viser, at de er polære. Følgende geometriske skitser viser, at de polære bindingsområdermetrisk arrangeret, så molekylet er polært. (Bemærk, at Le .isstrukturen ovenfor fejlagtigt antyder, at bindingerne er symmetrisk arrangeret.Husk, at Le .is strukturer ofte giver et falsk indtryk af geometrienaf de molekyler, de repræsenterer.)

e., Den nye struktur og geometriske skitse for HCN er de samme:
elektronegativiteten af hydrogen,carbon og nitrogen er 2,20, 2,55 og 3,04. 0,35 forskellen ielektronegativitet for H-C-bindingen viser, at den i det væsentlige er ikke-polær. Den 0,49 forskel i elektronegativitet for C-N-bindingen fortæller os, at den er polær.Molekyler med en polær binding er altid polære.