Peroxider er en gruppe af forbindelser med den struktur, R−O−O−R. O−O-gruppen i en peroxid er kaldet brintoverilte gruppe eller peroxo gruppe. I modsætning til O .idioner har O .ygenatomerne i Pero .idionen et O .idationstal på -1.,
-
InChI=1S/O2/c1-2/q-2Key: ANAIPYUSIMHBEL-UHFFFAOYSA-N
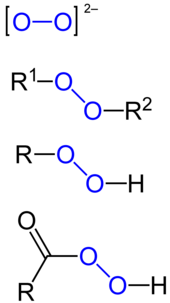
Types of peroxides, from top to bottom: peroxide ion, organic peroxide, organic hydroperoxide, peracid. The peroxide group is marked in blue. R, R1 and R2 mark hydrocarbon moieties.,
det mest almindelige pero .id er hydrogenpero .id (H2O2), almindeligvis kendt som “pero .id”. Det markedsføres som en opløsning i vand ved forskellige koncentrationer. Da hydrogenpero .id er næsten farveløst, er disse løsninger også. Det bruges hovedsageligt som O .idant og blegemiddel. Imidlertid produceres hydrogenpero .id også biokemisk i den menneskelige krop, stort set som et resultat af en række o .idaseen .ymer. Koncentrerede opløsninger er potentielt farlige, når de kommer i kontakt med organiske forbindelser.,

Bortset fra hydrogen peroxid, nogle af de store klasser af peroxider er:
- Peroxy syrer, den peroxy-derivater af mange velkendte syrer, eksempler er peroxymonosulfuric syre og pereddikesyre, og deres salte, et eksempel, som er kalium peroxydisulfate.
- hovedgruppe pero .ider, forbindelser med bindingen E−O−O−E (E = hovedgruppe element).,
- Metal peroxides, examples being barium peroxide (BaO2), sodium peroxide (Na2O2) and zinc peroxide (ZnO2).
- Organic peroxides, compounds with the linkage C−O−O−C or C−O−O−H. One example is tert-butylhydroperoxide.
