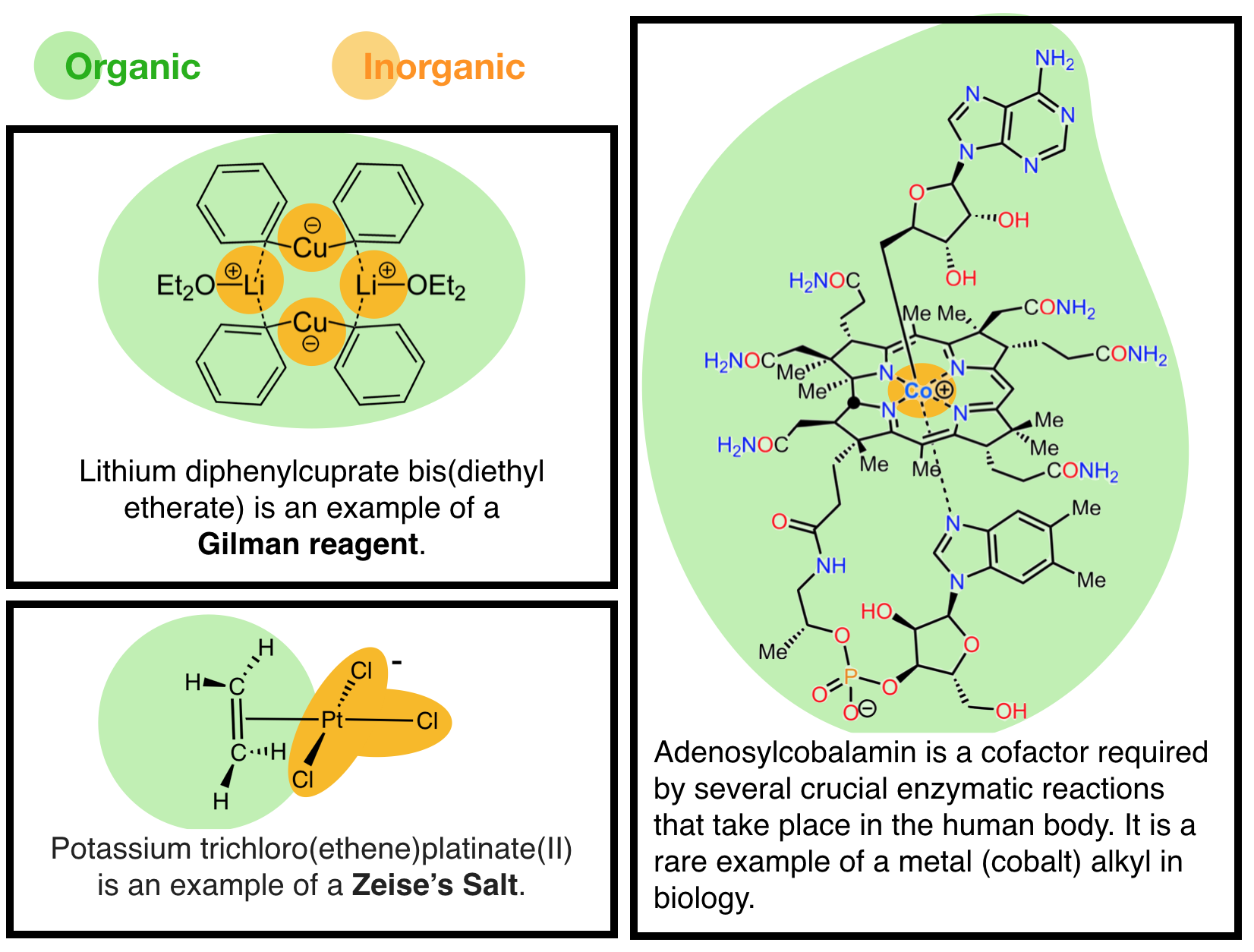
a divisão entre os campos da Química Inorgânica e orgânica tornou-se turva. Por exemplo, vamos olhar para uma das principais classes de catalisadores usados para reações de síntese orgânica; catalisadores organometálicos (figura \(\PageIndex{1}\)). Catalisadores organometálicos como estes, e todos os compostos organometálicos, contêm metais que estão ligados a moléculas contendo carbono ou carbono. Então, eles são “inorgânicos” porque contêm metais, ou” orgânicos ” porque contêm carbono?, Estes ilustram que divisões claras entre química orgânica e inorgânica não existem. Além disso, íons metálicos são comuns na biologia e assim a idéia de que os metais são “inorgânicos” e, portanto, classificados como “não-vivos ou não-biológicos” é incorreta. Um exemplo canônico é o catalisador organometálico, adenosilcobalbumina, que é um importante cofator biológico contendo um íon cobalto (Co) (figura \(\PageIndex{1}\), à direita) e uma ligação cobalto-carbono.
Alguns dos subcampos de Química Inorgânica foco na condutividade elétrica de materiais inorgânicos (ie condução, superconduction, e semiconduction) e no estudo de óptica e propriedades eletrônicas de compostos inorgânicos nanomateriais., A condutividade elétrica é uma propriedade canônica dos metais, mas os materiais à base de carbono também demonstram condutividade elétrica. Por exemplo, os nanotubos de carbono conduzem a electricidade através dos seus sistemas conjugados alargados \(\pi\). Fulerenos, dos quais o mais famoso é Buckminsterfulereno, ou Buckeyball (C60), demonstram propriedades interessantes que são semelhantes às nanopartículas, e quando combinado com metais e cristalizada pode demonstrar a supercondutividade.,
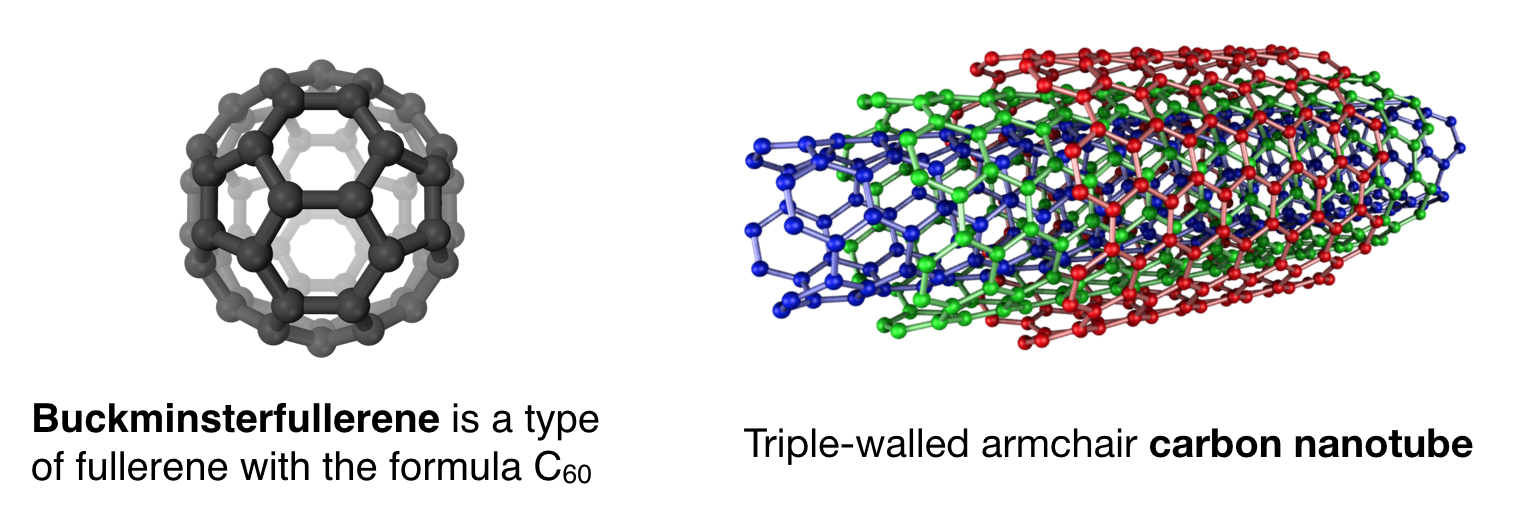
embora nanotubos de carbono e fullerenos sejam alótropos de carbono, suas propriedades materiais são um pouco estranhas a muitos químicos orgânicos, que tradicionalmente têm focado em moléculas orgânicas menores com propriedades muito diferentes., No entanto, estas propriedades são familiares aos químicos inorgânicos. Assim, químicos inorgânicos têm abraçado essas moléculas como” inorgânicas ” devido ao fato de que elas se comportam mais como materiais inorgânicos do que moléculas orgânicas menores. Esta classe de moléculas baseadas em carbono serve como outro exemplo de moléculas que não são perfeitamente compatíveis com as definições tradicionais de química “orgânica” e “inorgânica”. Certamente, o futuro deterá cada vez mais exemplos de moléculas que não se encaixam nas disciplinas tradicionais da química.
