Synthèse de l’Aspirine
de l’Aspirine ou de l’acide acétylsalicylique (AAS) est un dérivé de l’acide salicylique, qui est utilisé comme un analgésique pour diverses affections du corps tels que le mal de tête. L’aspirine présente des propriétés antiplaquettaires ou anticoagulantes en inhibant les prostaglandines, réparant ainsi les vaisseaux sanguins endommagés., Par conséquent, l’aspirine est utilisée à faibles doses à long terme dans le traitement des crises cardiaques, des accidents vasculaires cérébraux et chez les personnes présentant des risques élevés de formation de caillots sanguins. La synthèse de l’acétyl-salicylique anhydride de l’acide salicylique et de l’acide acétique anhydride acétique est catalysée par l’acide phosphorique. L’efficacité est estimée par le temps nécessaire pour terminer la réaction.
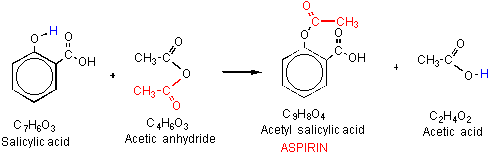
le Schéma 3.,flask
Ice cubes
Hot plate
Microwave oven
Stirring rod
Buchner funnel
Safety goggles
Stop watch
Experimental Procedure
18 ml of acetic anhydride was slowly added to 10 grams of salicylic acid in a 250 ml Erlenmeyer flask in the hood., 10 à 20 gouttes d’acide phosphorique à 85% ont été soigneusement ajoutées à la solution et bien mélangées. Le mélange a été chauffé sur une plaque chauffante jusqu’à ce que tout l’acide salicylique soit dissous. Une fois la réaction terminée, 20 gouttes d’eau distillée ont été prudemment ajoutées au mélange, suivies de 20 ml d’eau distillée. La solution a été refroidie sur un bain de glace jusqu’à ce que l’aspirine cristallise. En cas d’absence de formation de cristaux, les parois du flacon ont été rayées avec une tige d’agitation pour initier la cristallisation. Les cristaux ont été filtrés à l’aide d’un filtre Buchner et extraits à l’aide d’eau glacée., Le solide a ensuite été séché dans un four à 100 °C pendant environ 30 minutes, pesé et le rendement a été calculé. L’expérience a été répétée dans un four à micro-ondes et le rendement a été comparé. D’autres analyses pourraient inclure des mesures du point de fusion, de L’IR et de la RMN.

Figure 10. Représente le produit final obtenu après synthèse.
résultats et Discussion
les structures solides de l’acide salicylique ont été dissoutes en présence d’anhydride acétique catalysé par l’acide., Le mélange dissous sur le refroidissement produit des cristaux blancs d’aspirine. L’énergie correspondante consommée par chaque méthode de chauffage est tabulée ci-dessous.
le Tableau 5. L’énergie consommée pour la réaction de synthèse.
d’après les données présentées dans le tableau 5, la méthode de synthèse par micro-ondes s’est révélée plus efficace que la plaque chauffante. Figue. La figure 10 montre le produit final de l’aspirine obtenu après procédé de synthèse. Le processus de synthèse a été amélioré dans le cas de la méthode de chauffage par micro-ondes, économisant ainsi de l’énergie., Le procédé à micro-ondes a également donné une quantité de produit légèrement supérieure à celle de la plaque chauffante.
Le pourcentage de l’énergie économisée par le four à micro-ondes sur le four classique, telle qu’enregistrée par le compteur d’électricité,
![]()
