synteza aspiryny
aspiryna lub kwas acetylosalicylowy (ASA) jest pochodną kwasu salicylowego, który jest stosowany jako środek przeciwbólowy w przypadku różnych dolegliwości ciała, takich jak ból głowy. Aspiryna wykazuje właściwości przeciwpłytkowe lub przeciwzakrzepowe poprzez hamowanie prostaglandyn, a tym samym naprawę uszkodzonych naczyń krwionośnych., Stąd aspiryna jest stosowana w niskich dawkach w leczeniu zawałów serca, udarów mózgu i u osób o wysokim ryzyku powstawania skrzepów krwi. Synteza bezwodnika Acetylo salicylowego z kwasu salicylowego i bezwodnika octowego jest katalizowana przez kwas fosforowy. Wydajność jest szacowana przez czas potrzebny do zakończenia reakcji.
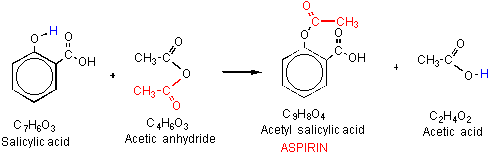
Schemat 3.,flask
Ice cubes
Hot plate
Microwave oven
Stirring rod
Buchner funnel
Safety goggles
Stop watch
Experimental Procedure
18 ml of acetic anhydride was slowly added to 10 grams of salicylic acid in a 250 ml Erlenmeyer flask in the hood., 10 do 20 kropli 85% kwasu fosforowego starannie dodano do roztworu i dokładnie wymieszano. Mieszaninę podgrzewano na gorącej płycie, aż do rozpuszczenia całego kwasu salicylowego. Po zakończeniu reakcji ostrożnie dodano 20 kropli wody destylowanej, a następnie 20 ml wody destylowanej. Roztwór był chłodzony w łaźni lodowej do czasu krystalizacji aspiryny. W przypadku braku tworzenia się kryształów ścianki kolby były porysowane mieszadłem w celu zainicjowania krystalizacji. Kryształy filtrowano za pomocą filtra Buchnera i ekstrahowano za pomocą schłodzonej wody., Następnie ciało stałe suszono w piekarniku w temperaturze 100 °C przez około 30 minut, zważono i obliczono wydajność. Eksperyment powtórzono w kuchence mikrofalowej i porównano wydajność. Dalsza analiza może obejmować temperaturę topnienia, pomiary IR i NMR.

Rysunek 10. Reprezentuje produkt końcowy otrzymany po syntezie.
wyniki i dyskusja
stałe struktury kwasu salicylowego rozpuszczono w obecności bezwodnika octowego, który jest katalizowany przez kwas., Rozpuszczona mieszanina po ochłodzeniu wytwarzała białe kryształy aspiryny. Odpowiednia energia zużywana przez każdą metodę ogrzewania jest tabelaryczna poniżej.
Tabela 5. Energii zużywanej do reakcji syntezy.
z danych przedstawionych w tabeli 5 wynika, że mikrofalowa metoda syntezy okazała się bardziej wydajna niż płyta grzejna. Rys. 10 pokazuje końcowy produkt aspiryny otrzymany po procesie syntezy. Proces syntezy został wzmocniony w przypadku mikrofalowej metody ogrzewania, oszczędzając w ten sposób energię., Proces mikrofalowy przyniósł również nieco większą ilość produktu niż płyta grzejna.
procent energii zaoszczędzonej przez kuchenkę mikrofalową w stosunku do konwencjonalnego piekarnika zapisany przez miernik mocy,
![]()
