limfocyty T odgrywają centralną rolę w ochronie człowieka przed wewnątrzkomórkowymi patogenami lub antygenami nowotworowymi, które wymagają odpowiedzi immunologicznej za pośrednictwem komórek T. Komórki T, w szczególności CD8+ komórki T, mogą być aktywowane do zabijania komórek nowotworowych lub zakażonych komórek po rozpoznaniu antygenów. Limfocyty T CD8+ składają się z 3 głównych podzbiorów, w tym limfocytów T naiwnych, efektorowych i pamięciowych. Naiwne limfocyty T są pierwotnymi limfocytami T, które wcześniej nie spotkały się z patogenem., Efektorowe limfocyty T są wytwarzane z wcześniej nieleczonych limfocytów T, gdy są narażone na działanie antygenów. Większość komórek efektorowych zostanie usunięta przez apoptozę po eliminacji patogenu w celu utrzymania równowagi immunologicznej.
jednak niewielka część długowiecznych komórek T pozostaje do szybkiej reakcji po ponownej ekspozycji na patogen. Ten rodzaj komórki nazywa pamięć T komórki. Ponieważ komórki pamięci T zostały przeszkolone do rozpoznawania specyficznych antygenów, wywołują szybszą i silniejszą odpowiedź immunologiczną po napotkaniu tego samego antygenu. W ten sposób szczepionki chronią nas przed infekcją.,
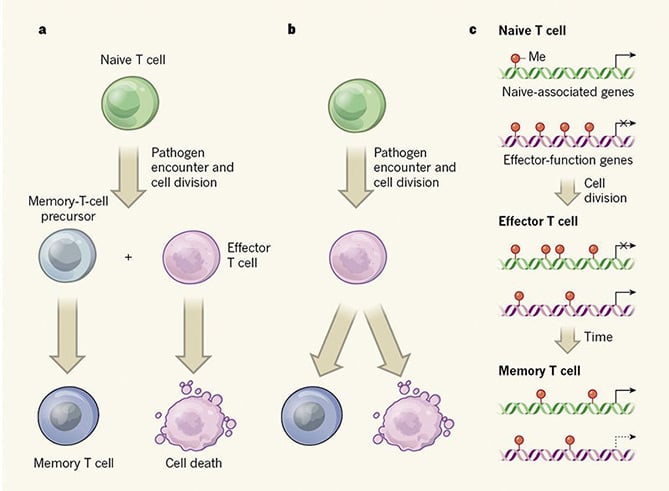
szczepionki były stosowane od wieków. Jednak nadal nie jest jasne, w jaki sposób komórki pamięci T są generowane, pomimo faktu, że jest to pole zaniżone. Zrozumienie pochodzenia komórek T pamięci będzie korzystne dla projektowania szczepionek. Zaproponowano dwa główne modele w celu wyjaśnienia mechanizmu leżącego u podstaw. Model A wspiera hipotezę, że komórki T pamięci pochodzą z naiwnych komórek T; Model B sugeruje, że podzbiór komórek efektorowych powoduje powstanie komórek T pamięci.
wreszcie, ta długotrwała debata ma teraz odpowiedź., Dwa zespoły badawcze, wspólnie z jednym liderem Dr Rafi Ahmed z Emory University School Of Medicine, opublikowały dwa artykuły online w Nature w tym tygodniu z silnymi dowodami zgodnymi z modelem B.
obie prace koncentrują się na szlaku przetwarzania komórek T CD8+. Akondy i in. wykorzystywane deuteru znakowane ludzkich komórek T po szczepieniu wirusem żółtej febry śledzić CD8 + komórek T, podczas gdy Youngblood et al. zastosowany model myszy do badania powstawania komórek T pamięci ., Sprawdzili epigenetyczne modyfikacje komórek T naiwnych, efektorowych i pamięciowych, a także konfigurację DNA w tych trzech typach komórek T.
metylacja DNA, jeden z rodzajów epigenetycznych zmian związanych z represją genów, został przeanalizowany przez Youngblooda i jego współpracowników. Okazało się, że metylacja DNA determinuje funkcję i status wśród trzech typów komórek T., Zarówno effector T komórki i pamięć T komórki mają podobny DNA metylowanie profile dla Effector funkcja geny z mniej metyl Grupa addycja porównywać naiwny T komórki, który sprzyja szybkiej odpowiedzi patogen re-ekspozycja dla pamięć T komórki. Ten silny dowód jest zgodny z Model B. Dodatkowo, pamięć T komórki potrzebują mniej metylacja naiwni-kojarzeni geny utrzymywać długo żywy etap po powstający od efektor T komórki. Autorzy dalej zidentyfikowali DNA metylotransferazy zwany Dnmt3a który reguluje T komórki etapy przez DNA metylacja.
Akondy i in., przeanalizowano również wzorce dostępności DNA i stwierdzono, że komórki pamięci t prezentują wzór dostępności chromatyny porównywalny do tego z efektorowymi komórkami T. Dostarcza to dalszych dowodów na poparcie idei, że komórki T pamięci powstają z komórek efektorowych.
oba badania wyraźnie wykazały, że limfocyty T pamięci są generowane z efektorowych komórek T poprzez modyfikacje epigenetyczne, a badania wykazały również, że Dnmt3a działa jako kluczowa metylotransferaza DNA wpływająca na tworzenie limfocytów T pamięci. To nowe odkrycie rzuca światło na lepszą strategię projektowania szczepionek., Ponadto przyczynia się do poprawy immunoterapii ukierunkowanej na Dnmt3a.
