T-lymfocytter spiller en central rolle i beskyttelsen af mennesker mod intracellulære patogener eller tumorantigener, der kræver t-cellemedierede immunresponser. T-celler, især CD8+ T-celler, kan aktiveres for at dræbe kræftceller eller inficerede celler efter genkendelse af antigener. CD8 + T-celler er sammensat af 3 store delmængder, herunder naive, effektor og hukommelse T-celler. Naive T-celler er de primære T-celler, der ikke har fundet patogen før., Effektor T-celler udvikles fra naive T-celler, når de udsættes for antigener. De fleste effektorceller fjernes gennem apoptose efter patogen eliminering for at opretholde immunbalancen.
en lille del af de langlivede T-celler forbliver dog stadig for hurtig respons ved patogenreeksponering. Denne type celler kaldes hukommelse T-celler. Fordi hukommelse T-celler er blevet trænet til at genkende specifikke antigener, vil de udløse en hurtigere og stærkere immunrespons efter at have mødt det samme antigen. Sådan fungerer vacciner for at beskytte os mod infektion.,
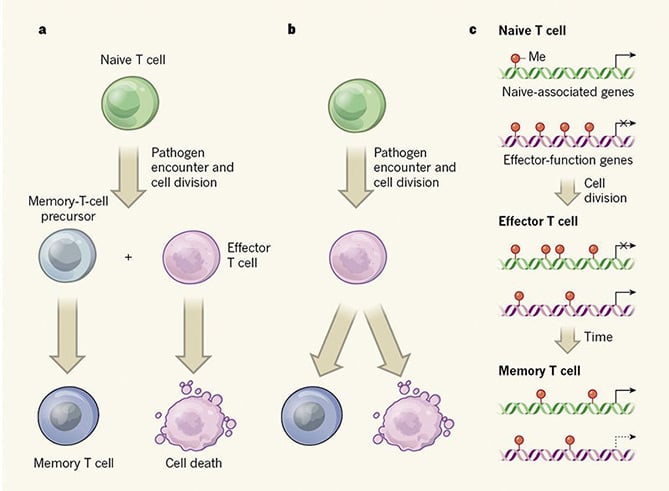
vacciner er blevet brugt i århundreder. Det er dog stadig uklart, hvordan hukommelse T-celler genereres på trods af det faktum, at det er et undervurderet felt. At forstå oprindelsen af hukommelse T-celler vil være gavnlig for vaccinedesign. To store modeller er blevet foreslået for at forklare mekanismen bag. Model A understøtter hypotesen om, at hukommelse T-celler er afledt af naive T-celler; Model B antyder, at en delmængde af effektorceller giver anledning til hukommelse T-celler.
endelig har denne langvarige debat et svar nu., To forskerteam, til fælles med en leder Dr. Rafi Ahmed ved Emory University School of Medicine, offentliggjorde to papirer online i Nature denne uge med de stærke beviser, der er enige med model B.
begge de to papirer fokuserer på CD8+ T-celler behandlingsvej. Akondy et al. udnyttet deuterium mærket humane T-celler efter gul feber virusvaccination for at spore CD8+ T-celler , mens Youngblood et al. ansat musemodel til at undersøge dannelsen af hukommelse T-celler ., De kontrollerede de epigenetiske modifikationer af naive, effektor og hukommelse T-celler, samt DNA-konfiguration i disse tre typer af T-celler.
DNA-methylering, en slags epigenetisk ændring, der er forbundet med genundertrykkelse, blev analyseret af Youngblood og hans kolleger. De fandt, at DNA-methylering bestemmer funktion og status blandt tre typer T-celler., Både effektor T-celler og hukommelse T-celler har lignende DNA-methyleringsprofiler for effektorfunktionsgener med mindre methylgruppetilsætning sammenlignet med naive T-celler, hvilket favoriserer hurtig respons på patogenreeksponering for hukommelse T-celler. Dette stærke bevis er i overensstemmelse med model B. Ud over, hukommelse T-celler har brug for mindre methylering af naive-associerede gener for at opretholde et langt levende stadium efter at have opstået fra effektor T-celler. Forfatterne identificerede yderligere en DNA-methyltransferase kaldet Dnmt3a, der regulerer t-celletrin gennem DNA-methylering.
Akondy et al., analyserede også mønstrene for DNA-tilgængelighed og fandt, at hukommelse T-celler præsenterer et kromatin-tilgængelighedsmønster, der kan sammenlignes med effektor T-celler. Dette giver yderligere beviser til støtte for tanken om, at hukommelse T-celler er opstået fra effektorceller.
begge undersøgelser viste tydeligt, at hukommelse T-celler genereres fra effektor T-celler gennem epigenetiske modifikationer, og undersøgelserne viste også, at Dnmt3a fungerer som en nøgle DNA-methyltransferase, der påvirker dannelsen af hukommelse T-celler. Denne nye fund kaster lys over en bedre vaccinedesignstrategi., Derudover bidrager det til forbedringen for immunterapier rettet mod Dnmt3a.
