Il y a eu une grande controverse et confusion dans la littérature lors de la discussion des dermatoses qui sont uniques à la grossesse. De nombreux noms différents ont été utilisés pour définir des troubles cliniquement similaires. Diverses classifications ont été proposées depuis la première contribution de Besnier en 1904 (Tableau 2).19
le Tableau 2.,Jaundice of pregnancy
Impetigo herpetiformis
Prurigo of pregnancy
Early onset prurigo of pregnancy
Papular dermatitis of pregnancy
Pruritic folliculitis of pregnancy
Polymorphic eruption of pregnancy
Polymorphic eruption of pregnancy (PEP) was first described by Lawley in 197920 as pruritic urticarial papules and plaques of pregnancy (PUPPP)., Les deux PEP et PUPPP sont des termes qui sont utilisés de manière interchangeable, avec PEP étant préféré dans la littérature actuelle. La PEP est la plus fréquente des dermatoses uniques à la grossesse, avec une incidence de 1 sur 160. Soixante-quinze à quatre-vingt-cinq pour cent des cas surviennent chez les primigravides, qui présentent un début prurigineux Brutal au cours du troisième trimestre de la grossesse, le plus souvent entre la 35e et la 39e semaine de gestation ou immédiatement après l’accouchement.21 l’éruption commence sur l’abdomen le long des stries distensae, épargnant la zone ombilicale et périumbilicale immédiate (fig. 7 et 8).,22 Ceci est en contraste avec la gestationis pemphigoïde, dans laquelle la majorité des cas surviennent dans la région ombilicale. La PEP peut se propager aux cuisses, aux fesses et aux extrémités, mais l’atteinte faciale est rare. Comme son nom l’indique, les manifestations cutanées sont assez variables. Il s’agit notamment de papules ou de plaques vésiculaires, de type cible, annulaires ou polycycliques qui deviennent confluentes avec le temps (Fig. 9 et 10). Trois catégories ont été définies23: type I, papules et plaques urticariennes; type II, érythème, papules ou vésicules Non urticariennes; et type III, combinaison de types I et II. la cause de la PPE est inconnue., Une théorie proposée est l’étirement rapide de la peau en fin de grossesse; cette hypothèse est corroborée par la présentation initiale de l’Éruption le long des stries distensae. L’augmentation du gain de poids chez la mère et le nouveau-né appuie cette théorie; il y a une incidence plus élevée de PPE dans les grossesses gémellaires.22, 24, 25
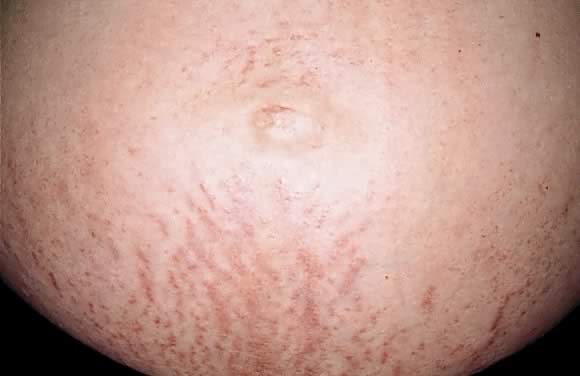 Fig. 7. Éruption polymorphe de la grossesse: papules érythémateuses le long des stries distensae.
Fig. 7. Éruption polymorphe de la grossesse: papules érythémateuses le long des stries distensae.
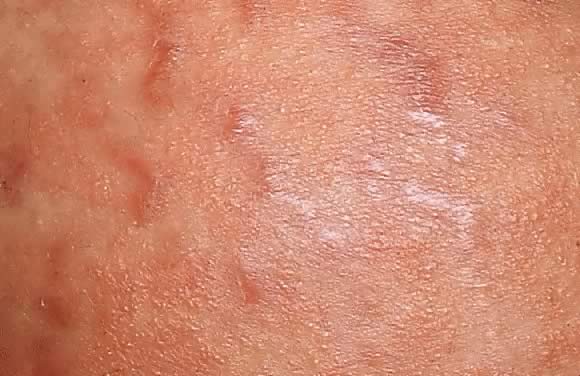 Fig. 8. Éruption polymorphe de la grossesse. Vue rapprochée de la Fig., 7 montrant les papules érythémateuses le long des stries distensae.
Fig. 8. Éruption polymorphe de la grossesse. Vue rapprochée de la Fig., 7 montrant les papules érythémateuses le long des stries distensae.
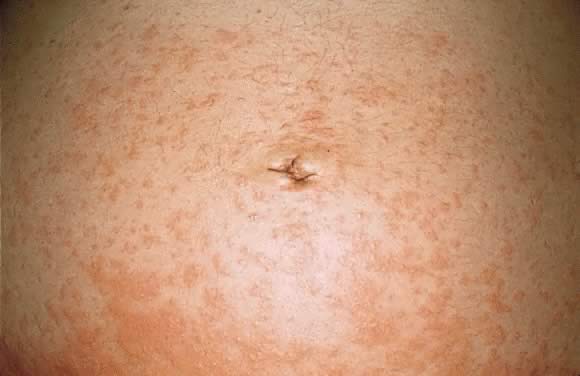 Fig. 9. Éruption polymorphe de la morphologie de la grossesse: papules urticariennes Coalescentes sur l’abdomen.
Fig. 9. Éruption polymorphe de la morphologie de la grossesse: papules urticariennes Coalescentes sur l’abdomen.
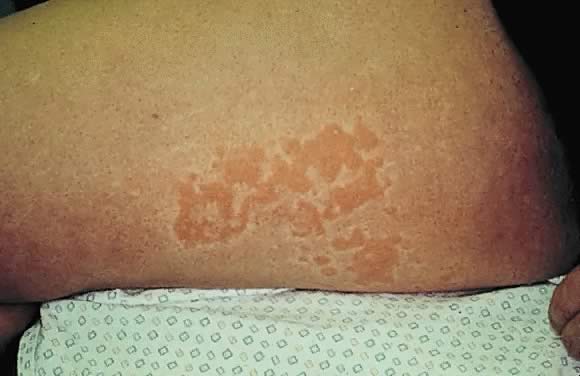 Fig. 10. Éruption polymorphe de la morphologie de la grossesse: plaques urticariennes sur la surface latérale du haut de la cuisse.
Fig. 10. Éruption polymorphe de la morphologie de la grossesse: plaques urticariennes sur la surface latérale du haut de la cuisse.
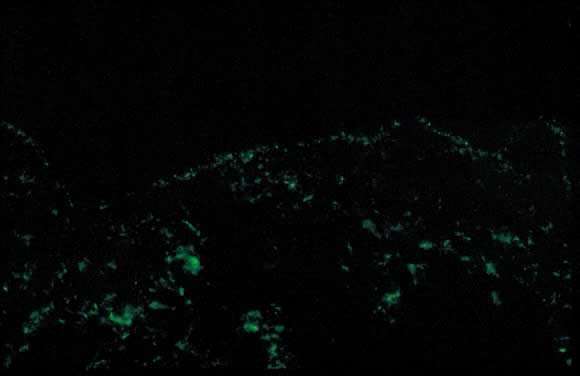 Fig. 11., Éruption polymorphe de grossesse immunofluorescence directe: bande granulaire de C3 le long de la zone de la membrane basale de la peau.
Fig. 11., Éruption polymorphe de grossesse immunofluorescence directe: bande granulaire de C3 le long de la zone de la membrane basale de la peau.
l’examen Dermatopathologique montre une spongiose épidermique variable avec un infiltrat inflammatoire périvasculaire dans le derme composé de lymphocytes, d’histiocytes et d’un nombre variable d’éosinophiles. L’immunofluorescence directe (DIF) est négative pour une bande linéaire de C3 ou D’IgG le long de la jonction dermoépidermique cutanée (DEJ); cependant, des dépôts D’IgM, de C3 et D’IgA ont été signalés le long de la DEJ et des vaisseaux sanguins sur DIF (Fig. 11).,23, 26 le diagnostic différentiel de la PPE comprend les gestations pemphigoïdes (PG), la dermatite de contact, l’Éruption médicamenteuse et les exanthèmes viraux. DIF de la peau est nécessaire pour différencier PEP de PG. L’évolution clinique de la PPE est généralement auto-limitante, avec une durée moyenne de 6 semaines. Le prurit est le plus grave au cours de la première semaine d’apparition, avec une rémission spontanée survenant dans les jours suivant la parturition. La mortalité maternelle et fœtale n’est pas affectée. La PPE survient rarement lors de grossesses subséquentes; cependant, quelques cas de récidive sont rapportés dans la littérature.,21 le traitement implique un soulagement symptomatique du prurit avec des corticostéroïdes topiques de faible à moyenne puissance (l’utilisation de corticostéroïdes à très forte puissance pendant une longue période doit être évitée) et des antihistaminiques de catégorie B pour la grossesse tels que la loratadine et la cétirizine. L’Hydroxyzine et la diphenhydramine sont des antihistaminiques de grossesse de catégorie C qui ont été utilisés pour soulager le prurit. En cas de prurit sévère ne répondant pas aux mesures conservatrices, l’administration systémique de corticostéroïdes ou l’administration induite est envisagée.,
gestationis Pemphigoïde
initialement décrite par Milton en 187222 comme « herpes gestationis”, cette affection a été renommée pemphigoïde gestationis (PG) en 1982 en raison de ses similitudes cliniques et d’immunofluorescence avec la pemphigoïde bulleuse.27 les deux noms continuent d’être utilisés; pemphigoid gestationis est plus commun au Royaume-Uni.28, 29
l’incidence estimée du PG est de 1 cas sur 50 000. La gestation pemphigoïde survient le plus souvent au deuxième ou au troisième trimestre de la grossesse; environ 25% des cas peuvent avoir une présentation initiale immédiatement après l’accouchement., La présentation clinique est un début brusque d’une éruption urticaire intensément prurigineuse sur le tronc qui forme des lésions vésicobulleuses tendues(Fig. 12 et 13). Environ 50% des cas ont une présentation initiale sur l’abdomen. L’atteinte ombilicale représente un nombre important de cas de PG. Comme dans PEP, atteinte de la membrane faciale et muqueuse I rare.29
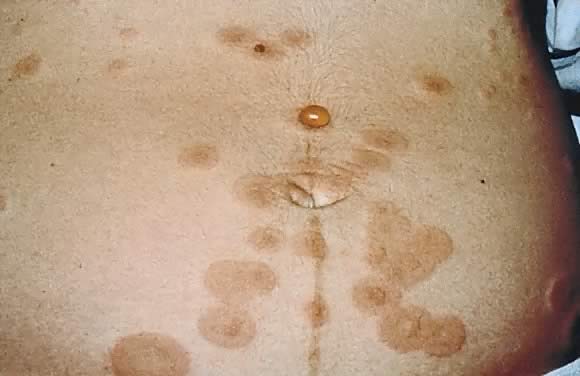 Fig. 12. Gestationis pemphigoïde: plaques urticariennes dans la zone périumbilicale avec des cloques tendues.
Fig. 12. Gestationis pemphigoïde: plaques urticariennes dans la zone périumbilicale avec des cloques tendues.
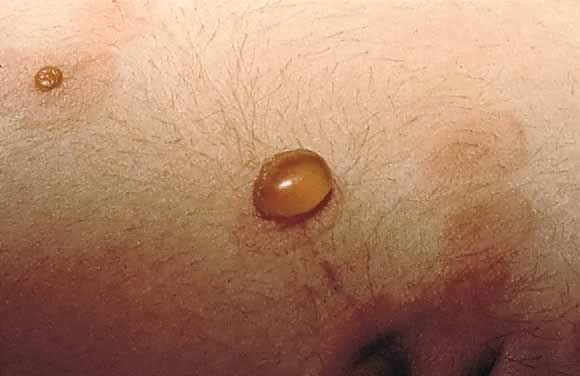 Fig. 13., Gestationis pemphigoïde: vue rapprochée de la boursouflure tendue sur la Fig. 12.
Fig. 13., Gestationis pemphigoïde: vue rapprochée de la boursouflure tendue sur la Fig. 12.
un diagnostic Précis est essentiel à la lumière de l’évolution clinique variable de ce trouble. La résolution spontanée au cours des semaines à des mois post-partum est un constat commun. Environ 75% des cas de PG présent avec des éruptions immédiatement post-partum. La récurrence dans les grossesses ultérieures avec un début plus précoce et une évolution clinique plus sévère est une caractéristique commune. Des grossesses sans maladie (c.-à-d. des « grossesses sautées”) sans atteinte cutanée chez des patientes ayant des antécédents de PG ont eu lieu., Il y a également eu des rapports de poussées de PG se développant avec la menstruation et l’utilisation de contraceptifs oraux (25% des cas).28, 29
PG est une maladie auto-immune causée par l’expression aberrante de L’antigène de classe MHC II sur les villosités choriales du placenta, qui déclenche une réponse allogène à la zone de la membrane basale placentaire et une réaction croisée subséquente avec la peau maternelle à travers le decidua maternel.30, 31 des cas de PG associés à une taupe hydatidiforme et à un choriocarcinome ont été rapportés.,32, 33 L’Association de PG avec d’autres maladies auto-immunes telles que la maladie de Graves a également été rapportée.34 études montrent également une incidence accrue dans HLA DR3 et DR4. HLA DR3 se produit dans le même pourcentage de personnes blanches que chez les personnes afro-américaines; cependant, le pourcentage de DR4 est plus faible chez les Afro-Américains, ce qui peut expliquer la rareté de PG dans cette population.35
l’examen Dermatopathologique de PG montre la formation de vésicules sous-épidermiques avec nécrose focale des kératinocytes., Le derme présente un œdème papillaire et un infiltrat périvasculaire constitué principalement d’éosinophiles et de quelques lymphocytes. Une découverte occasionnelle sur l’histopathologie est l’alignement des éosinophiles le long de la jonction dermoépidermique. DIF montre une bande linéaire caractéristique de C3 le long de la zone de membrane basale de la peau des patients atteints de PG (Fig. 14). Le dépôt linéaire de c3 sur DIF est un diagnostic de PG dans le cadre clinique correct et est utilisé pour différencier la PEP de la PG.36 en utilisant cette méthode, environ 25% des cas présentent également des dépôts D’IgG le long de la zone de membrane basale., L’immunofluorescence indirecte (IIF) démontre le « facteur PG”, qui consiste à faire circuler des anticorps anti-zone de membrane basale fixant le complément des IgG dans le sérum de patients atteints de PG. L’IIF activé par le complément à l’aide d’anticorps monoclonaux dirigés contre IgG1 démontre ce facteur chez tous les patients PG.37 cliniquement, les titres du facteur PG ne sont pas corrélés avec la gravité de la maladie. Le facteur PG est une IgG dirigée contre un composant hémidesmosomique (transmembranaire) de 180 kD de la zone membranaire basale.La microscopie électronique 38 montre également les dépôts de C3 et D’IgG dans la lamina lucida.,39
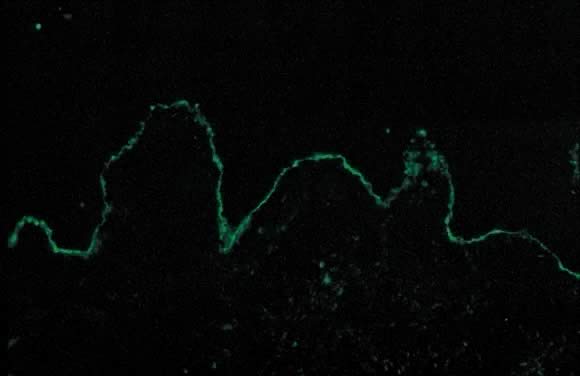 Fig. 14. Gestationis pemphigoïde par immunofluorescence directe: bande linéaire de C3 le long de la zone membranaire basale de la peau.
Fig. 14. Gestationis pemphigoïde par immunofluorescence directe: bande linéaire de C3 le long de la zone membranaire basale de la peau.
chez PG, 10% des nourrissons nés de mères touchées ont des lésions cutanées qui ressemblent à PG; ce n’est pas le cas avec la PPE. Les études DIF et IIF réalisées sur certains de ces nourrissons concordent avec un diagnostic de PG.29 l’évaluation de la morbidité et de la mortalité fœtales associées au PG a suscité de nombreuses controverses.,40 un consensus récent sur la morbidité infantile indique une légère augmentation de la prématurité et de la petite taille pour l’âge gestationnel.41, 42 le diagnostic différentiel de PG comprend la PPE, la dermatite de contact allergique et l’Éruption médicamenteuse. Un historique clinique précis accompagné de tests diagnostiques tels que l’histopathologie et le DIF permet de distinguer ces troubles. Les options de traitement comprennent des stéroïdes oraux (0,5 mg/kg par jour) avec une augmentation possible de la dose au moment de l’accouchement pour éviter les exacerbations post-partum., D’autres options incluent la plasmaphérèse, les corticostéroïdes topiques et les antihistaminiques, qui offrent tous des avantages limités. Après l’accouchement, selon le statut d’allaitement, d’autres traitements peuvent inclure la dapsone, le méthotrexate et la cyclosporine.29
impétigo herpétiformis
L’impétigo herpétiformis est une éruption aiguë de psoriasis pustuleux pendant la grossesse (se présentant le plus souvent au troisième trimestre) chez des personnes sans antécédents de psoriasis. Le premier cas a été décrit par Von Hebra en 1872; depuis lors, environ 100 cas ont été signalés.,43 la présentation clinique implique des pustules stériles sur une base érythémateuse qui deviennent progressivement plus confluentes.44 cette éruption commence généralement sur la peau en flexion et inguinale et se propage progressivement au tronc et implique la peau périumbilicale (fig. 15 et 16). Une atteinte de la membrane muqueuse de l’oropharynx et de l’œsophage est également observée., L’impétigo herpétiformis est associé à des symptômes constitutionnels tels qu’une température élevée; des symptômes gastro-intestinaux, notamment des nausées, des vomissements et de la diarrhée; des symptômes du système nerveux central tels que le délire; et la manifestation musculo-squelettique de la tétanie due à l’hypocalcémie.8, 45 éruptions récurrentes dans les grossesses ultérieures présentent généralement un début plus précoce et une évolution plus sévère.45 Il y a également eu des rapports d’exacerbation de cette condition chez les patients affectés associés à l’utilisation ultérieure de contraceptifs oraux.46
 Fig. 15., Impétigo herpétiformis: Éruption papulosquameuse érythémateuse diffuse sur le tronc et les extrémités.
Fig. 15., Impétigo herpétiformis: Éruption papulosquameuse érythémateuse diffuse sur le tronc et les extrémités.
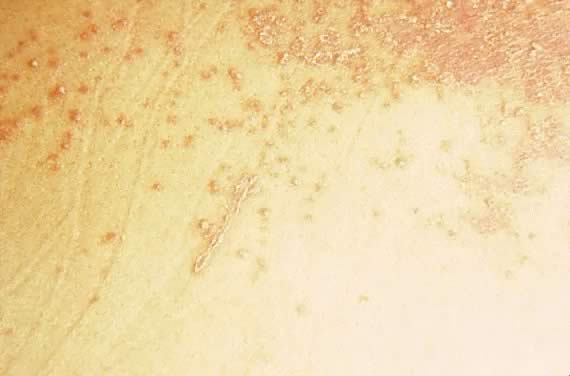 Fig. 16. Impétigo herpetiformis: papules érythémateuses Coalescentes avec écaille argentée.
Fig. 16. Impétigo herpetiformis: papules érythémateuses Coalescentes avec écaille argentée.
diagnostic Précoce et le traitement est important. Les quelques cas signalés sont associés à un risque accru de mortalité fœtale due à une insuffisance placentaire, à une augmentation des mortinaissances et à des anomalies fœtales.,45 les résultats de laboratoire comprennent des signes de leucocytose, un taux élevé de sédimentation érythrocytaire, une hypoalbuminémie et une hypocalcémie.8 l’examen histopathologique des échantillons de biopsie cutanée est compatible avec le psoriasis pustuleux. L’épiderme présente une parakératose et un allongement des crêtes de rete avec des pustules spongiformes de Kogoj. DIF, comme dans le psoriasis, est négatif.45
le traitement implique des corticostéroïdes oraux (avec un bénéfice limité), la correction de l’hypocalcémie, des mesures de soutien et des antimicrobiens pour prévenir les infections secondaires. L’interruption de grossesse est habituellement curatif.,45, 46 rétinoïdes (isotrétinoïne) et la luminothérapie sont des moyens de traitement plus efficaces qui peuvent être utilisés post-partum.
Cholestase de la grossesse,
la Cholestase de la grossesse a été initialement décrite par Svanborg47 et Thorling48 en 1954. La cholestase de la grossesse a été appelée par de nombreux autres noms, y compris prurigo gravidarum, cholestase intrahépatique de la grossesse, jaunisse de la grossesse et cholestase obstétricale. On pense que l’étiologie est multifactorielle et que la maladie survient dans 0,02 à 2,4% des grossesses., Des études montrent une incidence accrue parmi certains groupes ethniques, tels que certains Indiens D’Amérique du Sud. Il existe également une variation saisonnière de la prévalence de cette maladie, avec une incidence plus élevée pendant les mois d’hiver. Cinquante pour cent des cas sont considérés comme familiaux, et une association plus élevée a été observée dans les grossesses gémellaires.49, 50 un autre facteur possible qui contribue à la pathogenèse de cette condition est l’effet de l’œstrogène et d’autres hormones féminines sur le métabolisme et la sécrétion de la bile hépatique.,8, 49
la cholestase de la grossesse, comme son nom l’indique, ne survient que pendant la grossesse (le plus souvent au cours du troisième trimestre) et disparaît après l’accouchement, avec un taux de récurrence de 40 à 60% dans les grossesses ultérieures. La présentation clinique comprend un prurit généralisé sévère sans lésions cutanées primaires. Les excoriations secondaires dues au grattage peuvent être les seules constatations cutanées. L’étendue et la gravité du prurit fluctuent jusqu’au moment de l’accouchement.49, 51 le prurit le plus sévère survient la nuit.18 environ 20% des patients présentent un ictère léger., Cette condition est la deuxième cause la plus courante de l’ictère; l’hépatite virale est la cause la plus fréquente.29 les valeurs de laboratoire démontrent des niveaux élevés de sels biliaires, d’aminotransférases sériques, de phosphatase alcaline et de γ-glutamyl transpeptidase.49, 51 Comme il n’y a pas de lésions cutanées primaires, les résultats de biopsie cutanée pour l’histologie et le DIF sont normaux.
le prurit s’améliore considérablement après l’accouchement et une résolution complète est obtenue en quelques jours. Dans les cas où les symptômes persistent, d’autres causes de cholestase doivent être traitées.,49 Il y a eu des rapports de récurrence des symptômes avec l’utilisation de contraceptifs oraux.51 le diagnostic différentiel du prurit pendant la grossesse devrait inclure les infections parasitaires, les réactions cutanées allergiques et d’autres troubles métaboliques.
le pronostic fœtal et maternel montre une augmentation du travail prématuré et un faible poids à la naissance. Le fœtus et la mère courent un risque accru d’hémorragie intracrânienne et post-partum, respectivement, en raison d’une carence en vitamine K, ce qui entraîne des cas de malabsorption prolongée des graisses.,29, 51 les options de traitement vont du repos au lit, d’un régime faible en gras et d’émollients topiques dans les cas bénins à l’utilisation d’agents tels que la cholestyramine, l’acide ursodésoxycholique (UDCA) et la S-adénosyl-L-méthionine dans les cas plus graves. Des études ont montré de meilleurs résultats pour la mère et le nourrisson avec L’administration D’UDCA par rapport au placebo. Dans les cas graves, une surveillance fœtale et une césarienne peuvent être nécessaires.51
Nodulaire de la grossesse
Nodulaire de la grossesse a été initialement décrit par Besnier dans 190420 comme nodulaire gestationis., Il se produit généralement au cours du deuxième au troisième trimestre de la grossesse sous forme de papules érythémateuses excoriées discrètes sur le tronc et l’aspect extenseur des membres inférieurs (Fig. 17). L’incidence est d’environ 1 grossesse sur 300. La pathogenèse de cette éruption serait la présence d’atopie chez la femme enceinte. L’examen histolologique des échantillons de biopsie cutanée montre une parakératose et une acanthose légère avec un infiltrat inflammatoire mixte de neutrophiles et d’éosinophiles dans la zone périvasculaire. Les résultats DIF et les valeurs de laboratoire sont normaux., Il n’y a pas d’augmentation du risque fœtal ou maternel, et le traitement implique un soulagement symptomatique avec des corticostéroïdes topiques et des antihistaminiques.8, 29
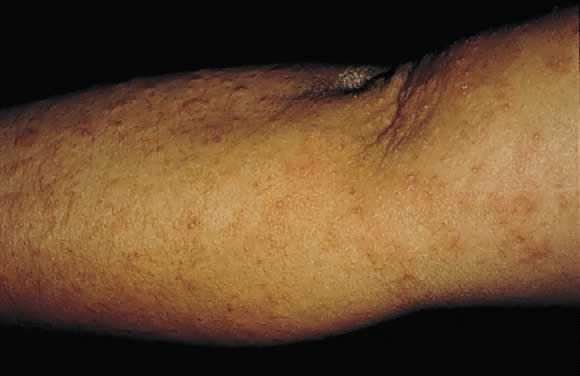 Fig. 17. Prurigo de grossesse: discrètes papules érythémateuses excoriées sur la surface extenseur du bras.
Fig. 17. Prurigo de grossesse: discrètes papules érythémateuses excoriées sur la surface extenseur du bras.
dermatite papuleuse de la grossesse
La dermatite papuleuse de la grossesse a été initialement décrite par Spangler en 196252 comme une éruption papuleuse érythémateuse et prurigineuse généralisée avec croûte centrale. La distribution est sur l’abdomen avec propagation aux extrémités., Une augmentation du taux d’hCG urinaire et une diminution du taux d’estriol urinaire, associées à une augmentation significative de la morbidité et de la mortalité fœtales, ont été initialement décrites. Beaucoup croient que la dermatite papuleuse de la grossesse et nodulaire de la grossesse sont des entités similaires. Les résultats histopathologiques et DIF sont similaires. Le risque fœtal élevé initialement signalé par Spangler52 n’a pas été reproductible dans d’autres études.53
folliculite prurigineuse de la grossesse
la folliculite prurigineuse de la grossesse a été décrite pour la première fois par Zoberman et Farmer en 1981.,54 le début de l’Éruption survient le plus souvent au cours du deuxième ou du troisième trimestre de la grossesse sous forme de petites papules érythémateuses autour des follicules. L’éruption est typiquement monomorphe avec une distribution sur le tronc et les extrémités (Fig. 18). L’examen histopathologique montre une folliculite et le DIF est négatif. Le diagnostic différentiel implique une dermatite papuleuse ou une acné induite par les stéroïdes. Le fœtus n’est pas affecté et le traitement comprend du peroxyde de benzoyle topique.8, 54
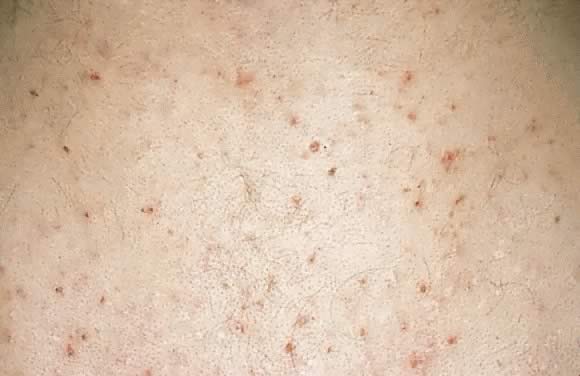 Fig. 18., Folliculite prurigineuse de la grossesse: papules érythémateuses centrées autour des follicules pileux sur le dos.
Fig. 18., Folliculite prurigineuse de la grossesse: papules érythémateuses centrées autour des follicules pileux sur le dos.
